
民以食为天,食品安全越来越受到大家的关注。下列有关说法正确的是
A.二氧化硫有毒,严禁将其添加到任何食品和饮料中
B.饮食“镉大米”会影响骨骼和肾脏,镉元素属于重金属元素
C.使用增塑剂——邻苯二甲酸酯可使聚氯乙烯由弹性塑胶变为硬塑胶
D.面粉生产中禁止添加的过氧化钙(CaO2)中阴阳离子的个数比为1:2
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:2015-2016学年江西省高安市高一下期中化学试卷(解析版) 题型:选择题
下列物质中,既含有离子键,又含有非极性键的是( )
A.Ca(OH)2 B.Na2O2 C.HClO D.H2O2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省等四校高二下第二次月考化学试卷(解析版) 题型:选择题
用一种试剂鉴别苯酚、己烯、碘化钾溶液、苯四种液体,可选用( )
A.盐酸 B.FeCl3溶液 C.溴水 D.四氯化碳
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三最后一卷理综化学试卷(解析版) 题型:实验题
非诺贝特(fenofibrate)是降胆同醇及甘油三酯的药物,它的一条合成路线如下:

已知:①羧酸类有机物与液溴在少量磷作用下,发生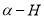 取代。
取代。

(1)B的名称为_______________。
(2)C所含官能团的名称为___________。
(3)写出下列物质的结构简式b_____________,F__________________。
(4)写出G到H的反应方程式_______________。
(5)写出同时符合下列条件的D的同分异构体结构筒式____________。
①能发生银镜反应;②含5种不同环境氢的联苯酯类有机物。
1 mol该有机物最多消耗NaOH的物质的量为_______________。
(6)以2-甲基丙烯为原料制备E,设计合成路线(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三最后一卷理综化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W在周期表中的相对位置如下图所示,已知它们的最外层电子数之和为21,下列说法一定正确的是
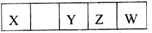
A.X、Y、Z、W中至少有一种是金属元素
B.元素的最高化合价:W>Z>Y
C.简单离子半径由大到小的顺序:W>Z>Y>X
D.一定条件下,W的单质可以置换出Z的单质
查看答案和解析>>
科目:高中化学 来源:2016届陕西西藏民族学院附中高三下考前三模理综化学试卷(解析版) 题型:实验题
硫酸铅可用于铅蓄电池、纤维增重剂、涂料分析试剂.工业上通常用自然界分布最广的方铅矿(主要成分为PbS)生产硫酸铅。工艺流程如下:
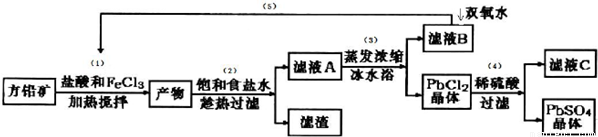
已知:①Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×l0-5.
②PbCl2(s)+2C1-(aq) PbCl42-(aq)△H>0
PbCl42-(aq)△H>0
③Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9和7.
(I )流程中加入盐酸可以控制溶液的pH<1.9,主要目的是___________,反应过程中可观察到淡黄色沉淀,则步骤(1)对应的主要反应的离子方程式为___________;
(II) 步骤(2)所得的滤液A 蒸发浓缩后再用冰水浴的目的是___________(请用平衡移动原理解释)
(III )上述流程中可循环利用的物质有___________;
(IV)炼铅和用铅都会使水体因重金属铅的含量增大而造成严重污染.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-。各形态的铅浓度分数α与溶液pH 变化的关系如图所示:
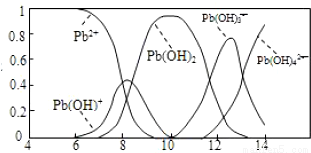
①探究Pb2+的性质:向含Pb2+的溶液中逐滴滴加NaOH,溶液变浑浊,继续滴加NaOH溶液又变澄清;pH≥13时,溶液中发生的主要反应的离子方程式为___________;
②除去溶液中的Pb2+:科研小组用一种新型试剂可去除水中的痕量铅和其他杂质离子,实验结果记录如下:
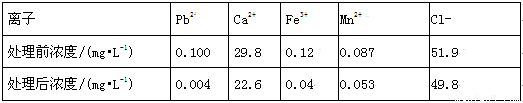
Ⅰ.新型试剂处理后的水中Pb2+浓度转化率为___________;
Ⅱ.若新型试剂(DH)在脱铅过程中主要发生的反应为:2DH(s)+Pb2+ D2Pb(s)+2H+,则脱铅时最合适的pH约为___________
D2Pb(s)+2H+,则脱铅时最合适的pH约为___________
A.4 B.6 C. 10 D. 12
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前周练模拟化学试卷(解析版) 题型:选择题
T1℃时,向容积为2L的密闭容器中充入一定量的X气体和Y气体,发生如下反应:X(g)+2Y(g) 3Z(g) 反应过程中测定的部分数据如下表:
3Z(g) 反应过程中测定的部分数据如下表:
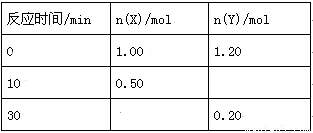
A.前10min内反应的平均速率为v(Z)=0.150 mol•L-1•min-1
B.若密闭容器体积可变,其他条件不变,在达到平衡后持续缩小容器体积,平衡后气体Y的物质的量保持不变
C.保持其他条件不变,起始时向容器中充入0.50molX气体和0.60moY气体,到达平衡时X转化率大于上述条件X转化率
D.温度为T2℃时(T1>T2),上述反应平衡常数为20,则正反应为放热反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学孔德校区高一下6月考化学卷(解析版) 题型:选择题
在光照条件下,CH4与Cl2能发生取代反应。若将1 mol CH4与Cl2反应,待反应完成后测得四种有机取代物的物质的量之比为n(CH3Cl)∶n(CH2Cl2)∶n(CHCl3)∶n(CCl4)=1∶2∶3∶4,则消耗的Cl2为
A.1.0 mol B.2.0 mol C.3.0 mol D.4.0 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com