
【题目】(1)常温下,在200 mL氢氧化钡溶液中含有1×10-3mol的钡离子,将此溶液与pH=3的盐酸混合,使其混合溶液的pH=7,应取氢氧化钡溶液和盐酸的体积之比是_________。
(2)25℃时,利用pH试纸测得0.1molL-1醋酸溶液的pH约为3,则可以估算出醋酸的电离常数约为_______;向10mL此溶液中加入少量冰醋酸,忽略溶解过程中溶液温度和体积的微小变化,溶液中c(H+)/c(CH3COOH)的值将_____(填“增大”、“减小”或“无法确定”)。
(3)25 ℃时,pH=3的NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=______(取近似值)
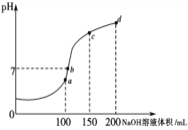
(4)室温时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系曲线如图所示:试分析图中a、b、c、d四个点,水的电离程度最大的是________点;在b点,溶液中各离子浓度由大到小的排列顺序是__________________________
【答案】 1:10 10-5mol·L-1 减小 10-3mol·L-1 a c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
【解析】(1)常温下,在200 mL氢氧化钡溶液中含有1×10-3mol的钡离子,则c[Ba(OH)2]=5![]() 10-3mol/L,c(OH-)=1
10-3mol/L,c(OH-)=1![]() 10-2mol/L。pH=3的盐酸中,c(H+)=1
10-2mol/L。pH=3的盐酸中,c(H+)=1![]() 10-3mol/L。混合后溶液的pH=7,因为c(OH-)=10 c(H+),则氢氧化钡溶液和盐酸的体积之比是1:10。
10-3mol/L。混合后溶液的pH=7,因为c(OH-)=10 c(H+),则氢氧化钡溶液和盐酸的体积之比是1:10。
(2)25℃时,利用pH试纸测得0.1molL-1醋酸溶液的pH约为3,c(H+)=![]() mol/L,则可以估算出醋酸的电离常数为
mol/L,则可以估算出醋酸的电离常数为![]() mol/L;向10mL此溶液中加入少量冰醋酸,忽略溶解过程中溶液温度和体积的微小变化,因为c(CH3COOH)变大后CH3COOH的电离程度变小,所以溶液中c(H+)/c(CH3COOH)的值将减小。
mol/L;向10mL此溶液中加入少量冰醋酸,忽略溶解过程中溶液温度和体积的微小变化,因为c(CH3COOH)变大后CH3COOH的电离程度变小,所以溶液中c(H+)/c(CH3COOH)的值将减小。
(3)25 ℃时,pH=3的NH4Al(SO4)2中,c(H+)=10-3mol·L-1、c(OH-)=10-11mol·L-1,由电荷守恒,得2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3mol·L-1-10-11mol·L-1![]() 10-3mol·L-1.
10-3mol·L-1.
(4)NH4HSO4溶液中,NH4HSO4完全电离,NH4HSO4= NH4++H++SO42-,溶液的酸性主要由其电离产生的H+决定的,水的电离受到其电离产生H+的抑制;当与反应2NH4HSO4+2NaOH=Na2SO4+ (NH4)2SO4+2H2O恰好完成时,因铵根离子水解溶液仍显酸性,但是铵根水解促进了水的电离,水的电离程度达到最大,此后继续加入NaOH溶液,溶液中铵根离子的浓度逐渐减小,溶液的pH逐渐增大,水的电离程度逐渐减小。由图可知,a、b、c、d四个点中,a点代表的是2NH4HSO4+2NaOH=Na2SO4+ (NH4)2SO4+2H2O恰好完成时,所以水的电离程度最大的是a点;在a点c(Na+)=2c(SO42-)->c(NH4+),则在b点,c(Na+)>2c(SO42-), 由pH=7得c(OH-)=c(H+),所以溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42)->c(NH4+)>c(OH-)=c(H+)。


 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
【题目】硼和铝位于同一主族,它们可以形成许多组成和性质类似的化合物.一种用硼镁矿(Mg2B2O5H2O)制取单质硼的工艺流程图如下: 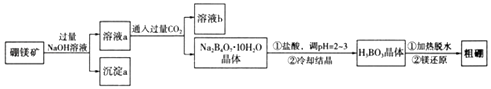
回答下列问题:
(1)Mg2B2O5H2O中B的化合价为 .
(2)溶液b中溶质的化学式为 .
(3)用pH试纸测溶液pH的操作方法是 .
(4)写出Mg2B2O5H2O与盐酸反应的化学方程式:
(5)制得的粗硼在一定条件下生成BI3 , BI3加热分解可以得到纯净的单质硼.现将0.0200g粗硼制成的BI3完全分解,生成的I2用0.3000mo1.L﹣1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液15.00mL.(已知:I2+2S2O32﹣=2I﹣+S4O62﹣)
①滴定操作中指示剂通常为
②该粗硼样品的纯度为 .
③若滴定管在使用前未用Na2S2O3标准溶液润洗,测得样品的纯度将(填“偏高”、“偏低”或“无影响”).
(6)请仿照如图形式设计从沉淀a中获得单质Mg的流程图(提示:在箭头上方或下方标出所用试剂或实验操作). ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某结晶水合物A含有两种阳离子和一种阴离子.将溶有90.60gA的水溶液分成两等份,向第一份逐滴加入NaOH溶液,溶液先出现白色沉淀后完全溶解,此过程中产生2.24L(标准状况)刺激性气味的气体.向第二份加入过量的Ba(OH)2溶液,过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.60g. 请回答以下问题:
(1)A的摩尔质量为 .
(2)试通过计算确定该结晶水合物的化学式为 .
(3)若第二份加入75.00mL2.00molL﹣1的Ba(OH)2溶液,则得到的沉淀质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,按强电解质、弱电解质、非电解质的顺序排列的是
A. NaCl、BaSO4 、SO2
B. Cu、CH3COOH、酒精
C. 氯化钠晶体、水、酒精
D. KNO3、NH3·H2O、CaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前国际上使用的“海水淡化”主要技术之一是蒸馏,将海水变成蒸汽,蒸汽经过冷却得到淡水,剩余的溶液可用来提取氯化钠、氯化镁等多种工业原料.工业上用电解熔融NaCl或MgCl2的方法分别制备金属钠和镁,同时得到氯气.
(1)若金属钠长期暴露在空气中,最终转化为 , 取一定量的该物质溶于水配制成饱和溶液,通入CO2气体后发现溶液变浑浊,写出发生反应的化学方程式 .
(2)若金属钠着火,不能用干冰灭火器灭火,原因是(用化学方程式表示) .
若金属镁着火,也不能用干冰灭火器灭火,原因是(用化学式表示)
(3)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
写出反应②的化学方程式;
写出反应④的化学方程式 .
氯气排放会污染环境,可用NaOH溶液来吸收Cl2 , 写出该反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:下列说法不正确的是
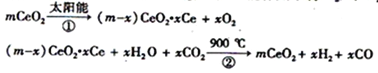
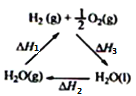
A. 该过程中CeO2没有消耗
B. 该过程实现了太阳能向化学能的转化
C. 右图中△H1=△H2+△H3
D. 以CO和O2构成的碱性燃料电池的负极反应式为:CO+4OH—- 2e—=CO32—+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物CH3﹣CH═CH﹣Cl能发生( ) ①取代反应 ②加成反应 ③消去反应 ④使溴水褪色 ⑤使KMnO4酸性溶液褪色 ⑥与AgNO3溶液生成白色沉淀 ⑦聚合反应.
A.以上反应均可发生
B.只有⑥不能发生
C.只有⑦不能发生
D.只有②不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 蔗糖、油脂、蛋白质都可以水解
B. 医用消毒酒精中乙醇的浓度为95%
C. Fe(OH)3不能通过化合反应得到
D. 交警用酸性重铬酸钾检查司机饮酒过量时乙醇发生了取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com