
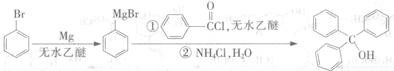
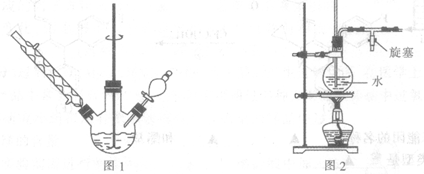
科目:高中化学 来源:不详 题型:填空题
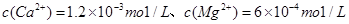 、
、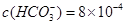
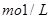 。要软化10 m3这种天然水,需先加入Ca(OH)2 g,再加入Na2CO3 g。
。要软化10 m3这种天然水,需先加入Ca(OH)2 g,再加入Na2CO3 g。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验目的 | 实验步骤及现象 |
| A | 检验亚硫酸钠试样是否变质 |  |
| B | 检验某卤代烃是否是氯代烃 |  |
| C | 证明酸性条件H2O2氧化性比I2强 |  |
| D | 除去铁屑表面的油污 | 铁屑用热的碳酸钠溶液洗涤,再用蒸馏水冲洗干净 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验 | P2O5 /g | 95%乙醇量/ mL | 加热方式 |
| 实验1 | 2 | 4 | 酒精灯 |
| 实验2 | 2 | 4 | 水浴70℃ |
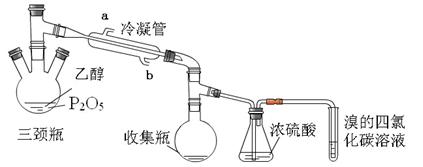
| 实验 | 实验现象 | ||
| 三颈瓶 | 收集瓶 | 试管 | |
| 实验1 | 酒精加入时,立刻放出大量的白雾,开始有气泡产生,当用酒精灯加热时,气泡加快生成并沸腾,生成粘稠状液体。 | 有无色液体 | 溶液褪色 |
| 实验2 | 酒精加入时,有少量白雾生成,当用水浴加热时,不产生气泡,反应一个小时,反应瓶内生成粘稠状液体 | 有无色液体 | 溶液不褪色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
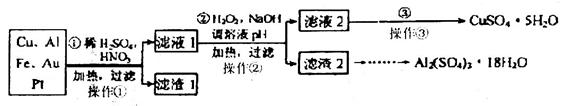
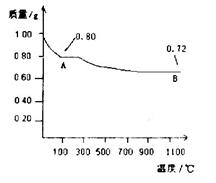
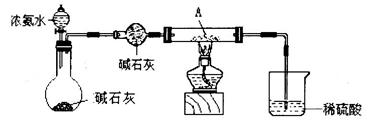
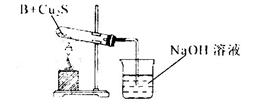
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.苯中含有苯酚杂质:加入溴水,过滤 |
| B.乙醇中含有乙酸杂质:加入碳酸钠溶液,分液 |
| C.FeCl3溶液中含有CuCl2杂质:加入过量铁粉,过滤 |
| D.CO2中含有HCl杂质:通入饱和NaHCO3溶液,洗气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
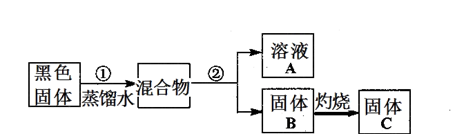
| 实验操作 | 预期现象 | 结论 |
| 步骤1:各取少量溶液A分装a、b、c三支试管,往a试管,__ __________________________ | 有白色沉淀产生 | 说明溶液A含有Cl- |
| 步骤2:往b试管,__________ __________________________ | ______________________ | _______________________ |
| 步骤3:往c试管,__________ __________________________ | 先产生_______________, 后____________________ | 说明溶液A含有Zn2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HCl、CuSO4、Mg(NO3)2、KOH | B.NaBr、AgNO3、HCl、Na2CO3 |
| C.H2SO4、NaCl、Na2SO4、Na2CO3 | D.NaOH、MgSO4、Na2CO3、KHSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com