
| A. | HCl | B. | CH4 | C. | CH2=CH2 | D. | Cl2 |
分析 只能用排水法收集,说明该气体能够与空气中的成分发生化学反应或者气体的密度与空气的密度接近,且该气体不与水发生反应、不易溶于水,据此进行判断.
解答 解:A.氯化氢极易溶于水,不能用排水法收集,可以使用排空气法收集,故A错误;
B.CH4不溶于水,密度比空气小,既可以用排水法收集,也可以用向下排气法收集,故B错误;
C.CH2=CH2的式量为28,空气的平均式量为29,乙烯的密度和空气接近,不能用排气法收集,只能用排水法收集,故C正确;
D.Cl2能溶于水且与水反应,因此Cl2不能用排水法收集,故D错误;
故选C.
点评 本题考查气体的收集方法,题目难度不大,注意实验室收集气体选择依据气体本身的密度、溶解性等物理性质,能用排水法收集的气体应为难溶于水且不与水反应的气体.


科目:高中化学 来源: 题型:多选题
| A. | 煤加强热而分解的过程叫做煤的干馏 | |
| B. | 煤干馏的目的是得到冶金用的优质焦炭 | |
| C. | 煤的干馏和石油的分馏的本质差别是:干馏是化学变化,而分馏是物理变化 | |
| D. | 工业上芳香烃原料可由煤干馏得到,其存在于干馏所得的焦炉气中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中有物质变化也有能量变化 | |
| B. | 化学键断裂吸收能量,化学键生成放出能量 | |
| C. | 需要加热的化学反应不一定是吸热反应 | |
| D. | 图所示的反应为放热反应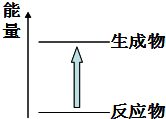 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
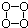 ),有关O4的说法正确的是( )
),有关O4的说法正确的是( )| A. | O4的摩尔质量是64g | |
| B. | O4和O2互为同位素 | |
| C. | 相同质量的O4与O3所含原子个数比为4:3 | |
| D. | O4与O3、O2都是氧元素的同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | W |
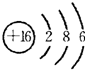 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素氧化物对应水化物的酸性一定强于Y | |
| C. | X元素形成的单核阴离子还原性强于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 4Z | B. | 4Z+6 | C. | 4Z+10 | D. | 4Z+14 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com