
煤化工中常需研究不同温度下平衡常数、投料比等问题。
已知:CO (g) +H2O
(g) H2
(g) +CO2 (g)平衡常数K随温度的变化如下表:
H2
(g) +CO2 (g)平衡常数K随温度的变化如下表:

回答下列问题
(1)该反应的平衡常数表达式K= ,ΔH= 0(填“<”、“>”、“=”)
(2)已在一定温度下,C(s) +CO2 (g) 2CO
(g)平衡常数K1;
2CO
(g)平衡常数K1;
C (s) +H2O(g) CO(g)
+H2 (g)平衡常数K2则K、K1 、K2,之间的关系是 :
CO(g)
+H2 (g)平衡常数K2则K、K1 、K2,之间的关系是 :
(3)8000C时,向一个10L的恒容反应器中充入0.40molCO和1.60mol水蒸气,经一段时间后反应达到平衡,此时CO的转化率为 :若保持其他条件不变,向平衡体系中再通入0. 10molCO和0.40molCO2,此时v正 v逆 (填“>”、“=”或“<”)。
(7分)(1) C(CO2 )C(H2)/C(CO) C(H2O),(1分) ,< (1分);
(2) K=K2/K1 (1分) (3)80% (2分);=(2分)
【解析】
试题分析:(1)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应的化学方程式可知,该反应的平衡常数表达式K=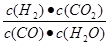 。根据表中的数据可知,随着温度的升高,平衡常数K是减小的,这说明升高温度平衡向逆反应方向进行,所以正方应是放热反应,即△H<0。
。根据表中的数据可知,随着温度的升高,平衡常数K是减小的,这说明升高温度平衡向逆反应方向进行,所以正方应是放热反应,即△H<0。
(2)根据盖斯定律可知,②-①即得到反应CO (g) +H2O (g) H2
(g) +CO2 (g),所以平衡常数之间的关系是K=K2/K1。
H2
(g) +CO2 (g),所以平衡常数之间的关系是K=K2/K1。
CO (g) +H2O (g) H2
(g) +CO2 (g)
H2
(g) +CO2 (g)
起始浓度(mol/L) 0.040 0.16 0 0
转化浓度(mol/L) x x x x
平衡浓度(mol/L) 0.040-x 0.16-x x x
则根据该温度下的平衡常数可知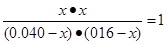
解得x=0.032mol/L
所以CO的转化率=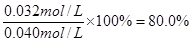
若保持其他条件不变,向平衡体系中再通入0. 10molCO和0.40molCO2,则此时CO、H2O、CO2、H2的浓度分别是(mol/L)0.018、0.128、0.072、0.032,所以Q=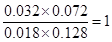 ,所以反应仍然是平衡状态,则正逆反应速率相等。
,所以反应仍然是平衡状态,则正逆反应速率相等。
考点:考查可逆反应平衡常数的计算、判断和应用
点评:该题是中等难度的试题,也是高考中的常见题型。试题针对性强,主要是考查学生对平衡常数含义、表达式以及有关应用的熟悉了解程度,旨在培养学生的逻辑思维能力和规范答题能力。在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| [H2]?[CO2] |
| [CO]?[H2O] |
| [H2]?[CO2] |
| [CO]?[H2O] |
| A | B | C | D | |
| n(CO2) | 3 | 1 | 0 | 1 |
| n(H2) | 2 | 1 | 0 | 1 |
| n(CO) | 1 | 2 | 3 | 0.5 |
| n(H2O) | 5 | 2 | 3 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 427 | 700 | 800 |
| 平衡常数 | 9.94 | 9 | b | 0.64 |
| 反应时间/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| A | B | C | D | |
| n(CO2)/mol | 3 | 1 | 0 | 1 |
| n(H2)/mol | 2 | 1 | 0 | 1 |
| n(CO)/mol | 1 | 2 | 3 | 0.5 |
| n(H2O)/mol | 5 | 2 | 3 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 H2(g)+CO2(g)的平衡常数随温度的变化如表:
H2(g)+CO2(g)的平衡常数随温度的变化如表:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
 2CO(g)平衡常数K;
2CO(g)平衡常数K; CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1; H2(g)+CO2(g) 平衡常数K2,
H2(g)+CO2(g) 平衡常数K2,| K1 |
| K2 |
| K1 |
| K2 |
| 4 |
| 9 |
| 4 |
| 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
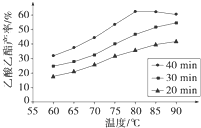 Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)
Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)| 浓H2SO4 |
| △ |
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com