

 ��������ע��������
��������ע��������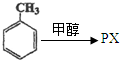
 ��������ע��������
��������ע�������� ��
�� ���� ��1���Զ��ױ�������ͬϵ����б���ͬϵ������ʣ�
��2���Զ��ױ������ϵ��ĸ���ԭ�ӵ�Ч�������ϵ�������ԭ�ӵ�Ч�����Է����ص���Ϊ6��4��
��3����2��-COOH�뺬2��-OH���л�������ϾۺϷ�Ӧ��
��4�����뻥�ܵĻ���������������ķ�����
��5����������д����Ӧ���PX�����ԭ���غ�ķ���д��С���ӣ�
��6�����ݺ�����ͬ�Ĺ����ţ���һ�ȴ��������֣���֪���ڱ������ᣮ
��� �⣺��1���Զ��ױ�������ͬϵ����б���ͬϵ������ʣ��������ɷ����ӳɷ�Ӧ���ұ����ϵ�H�����ϵ�H�ɷ���ȡ����Ӧ����ȼ�ռ���ǿ�������������ɷ���������Ӧ���ʴ�Ϊ��ȡ����Ӧ��������Ӧ��
��2���ɶԳ��Կ�֪���Զ��ױ������ϵ��ĸ���ԭ�ӵ�Ч�������ϵ�������ԭ�ӵ�Ч��PX�ĺ˴Ź���������2��壬�ҷ����ص���Ϊ6��4��3��2��
�ʴ�Ϊ��2��6��4��3��2��
��3����2��-COOH�뺬2��-OH���л�������ϾۺϷ�Ӧ���÷�ӦΪ ��
��
�ʴ�Ϊ�� ��
��
��4��������и���ֻ��ܣ����е㲻ͬ�����ú�����з����ᴿ�Զ��ױ��ķ��������ʴ�Ϊ������
��5�����ױ��״���������Ʊ��Զ��ױ���PX������Ӧ����ˮ����ӦΪ ��
��
�ʴ�Ϊ�� ��
��
��6��PTA��һ��ͬ���칹��X���京����ͬ�����ţ����䱽���ϵ�һ��ȡ���������֣���֪XΪ�ڱ������ᣬ������X��1��3-������1��1�γ�������Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼���л���ĺϳɼ��ṹ�����ʣ�Ϊ��Ƶ���㣬���չ����������ʵĹ�ϵ��ϰ���е���ϢӦ��Ϊ���Ĺؼ������ط�����Ǩ��Ӧ���������ۺϿ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 20��5 mL 0.1 mol•L-1��Na2S2O3��Һ��10mL 0.1 mol•L-1��H2SO4��Һ��5mL H2O | |
| B�� | 20��5 mL 0.2mol•L-1��Na2S2O3��Һ��5 mL 0.2 mol•L-1��H2SO4��Һ��10mLH2O | |
| C�� | 30��5mL0.1 mol•L-1��Na2S2O3��Һ��10mL 0.1 mol•L-1��H2SO4 ��Һ��5mLH2O | |
| D�� | 30��5 mL0��2 mol•L-1��Na2S2O3��Һ��5 mL 0.2 mol•L-1��H2SO4��Һ��10mL H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ���þ����к�����������У����Ӽ��ͷǼ��Լ���
���þ����к�����������У����Ӽ��ͷǼ��Լ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �ϳɰ���Ӧ��N2��g��+3H2��g��?2NH3��g������H��0��Ϊʹ���IJ�����ߣ�������Ӧ��ȡ���¸�ѹ�Ĵ�ʩ | |
| B�� | ��2HI��g��?H2��g��+I2��g��ƽ����ϵ����ѹǿʹ��ɫ���� | |
| C�� | SO2��������SO3�ķ�Ӧ��������Ҫʹ�ô��� | |
| D�� | ��֪��Ӧ2NO2��g��?N2O4��g��������ɫ����NO2��ѹ����ɫ�ȱ�����dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ���������Ƭ�ϣ�2Fe+6H+�T2Fe3++3H2�� | |
| B�� | ����ͭ��Һ������������Һ��ϣ�CuSO4+2OH-�TCu��OH��2��+SO42- | |
| C�� | ̼��������Һ��ϡ�����ϣ�HCO3-+H+�TH2O+CO2�� | |
| D�� | ��������Һ���Ȼ�����Һ��ϣ�AgNO3+Cl-�TAgCl��+NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2O2�ĵ���ʽ��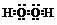 | B�� | ��ԭ�ӵĽṹʾ��ͼ��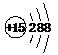 | ||
| C�� | �Ҵ��Ľṹʽ��C2H6O | D�� | ����Ľṹ��ʽ��C2H4O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
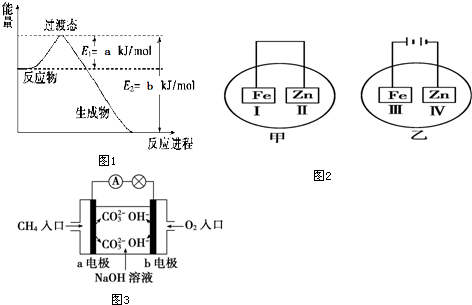
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com