
下列关于铷的叙述不正确的是( )
|
| A. | 金属铷投入水中会引起爆炸 |
|
| B. | 铷是一种强还原剂,铷离子很稳定 |
|
| C. | 铷受热后,能在空气中剧烈燃烧,生成比过氧化物更复杂的氧化物 |
|
| D. | 铷原子的核电荷数比钾原子的核电荷数多,因此铷原子失电子的能力小于钾原子 |
| 碱金属的性质.. | |
| 分析: | Rb属于碱金属族元素,位于Na元素下方,所以其金属性大于Na, A.Rb与水反应比Na更剧烈; B.金属元素单质的还原性越强,其简单阳离子氧化性越弱; C.Rb金属性比K更强,能在空气中燃烧; D.同一主族金属元素,其单质的还原性随着原子序数增大而增强,则失电子能力越强. |
| 解答: | 解:Rb属于碱金属族元素,位于Na元素下方,所以其金属性大于Na, A.Rb与水反应比Na更剧烈,钠与水反应发出嘶嘶声音,则Rb和水反应会引起爆炸,故A正确; B.金属元素单质的还原性越强,其简单阳离子氧化性越弱,Rb的还原性大于Na,则简单铷离子氧化性很弱,所以其简单离子很稳定,不易被还原,故B正确; C.Rb金属性比K更强,能在空气中燃烧,K燃烧生成超氧化物,则Rb燃烧生成比过氧化物更复杂的氧化物,故C正确; D.同一主族金属元素,其单质的还原性随着原子序数增大而增强,则失电子能力越强,所以铷原子失电子的能力大于钾原子,故D错误; 故选D. |
| 点评: | 本题考查碱金属族元素,明确同一主族元素性质递变规律是解本题关键,以碱金属族、卤族元素为例熟练掌握同一主族元素性质递变规律及其原因,题目难度不大. |


科目:高中化学 来源: 题型:
用坩埚钳夹住一小块刚用酸处理过的铝箔,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于实验现象的解释不正确的是( )
A.铝在空气中能很快形成氧化膜 B.氧化铝薄膜兜住了熔化的铝
C.氧化铝的熔点比铝高 D.铝箔表面温度低,未熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
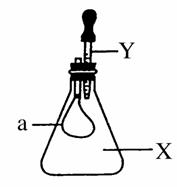
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压胶头滴管,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起。气体X和液体Y不可能是( )
A.X是HCl,Y是饱和食盐水
B.X是CO2,Y是稀H2SO4
C.X是SO2,Y是NaOH溶液
D.X是NH3,Y是NaNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中正确的是( )
A.蒸馏实验中,温度计水银球应位于蒸馏烧瓶支管口处
B.制备乙酸乙酯的实验中,导管末端要伸入饱和Na2CO3溶液液面下
C.分液操作中,待下层液体流出后,再将上层液体从分液漏斗下口放出
D.测定溶液pH时,可用pH试纸蘸取少量待测液,并与标准比色卡比较
查看答案和解析>>
科目:高中化学 来源: 题型:
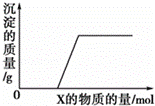
将溶液(或气体)X逐渐加入(或通入)到一定量的Y溶液中,产生沉淀的质量与加入X的物质的量关系如图所示,符合图中情况的一组物质是( )
| X | Y溶液 | |
| A | Ba(HCO3)2溶液 | NaOH溶液 |
| B | KOH溶液 | Mg(HSO4)2溶液 |
| C | Na2CO3溶液 | CaCl2溶液 |
| D | CO2气体 | 石灰水 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2O2、HCl、Al2O3 三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl﹣、OH﹣;且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为( )
|
| A. | 3:2:1 | B. | 2:4:1 | C. | 2:3:1 | D. | 4:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作不能达到目的的是( )
| 选项 | 目的 | 操作 |
| A | 配制100 mL 1.0 mol·L-1 CuSO4溶液 | 将25 g CuSO4·5H2O溶于100 mL蒸馏水中 |
| B | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C | 在溶液中将MnO | 向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 |
| D | 确定NaCl溶液中是否混有Na2CO3 | 取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com