
【题目】0.1 mol CaCl2固体中含有
A.0.1 mol Cl2B.1.204×1024个ClC.0.1 mol Ca2+D.3.01×1023个Ca2+
科目:高中化学 来源: 题型:
【题目】已知A是一种只含碳、氢、氧三种元素的有机物,其蒸气的密度为相同条件下的氢气的密度的23倍。A可以和金属钠反应放出氢气并在一定条件下发生如图所示的变化。回答下列问题:
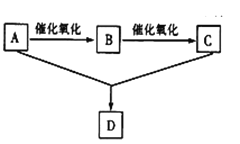
(1)A的结构简式为:__________,D的名称是___________,
(2)C中官能团名称________,A+C→D的反应类型__________,
(3)写出反应的化学方程式:
A→B_______
A+C→D_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的主要组成元素是碳、氢、氧、硫、氮,燃煤产生CxHy、SO2等大气污染物,煤的气化是高效、清洁利用煤炭的重要途径之一。回答下列问题:
(1)利用煤的气化获得的水煤气( 主要成分为CO、CO2和H2 )在催化剂作用下可以合成绿色燃料甲醇。
已知: H2O(1) = H2O(g) ΔH1= +44 .0kJ/mol
CO2(g)+H2(g) = CO(g)+H2O(l) ΔH2=-3.0kJ/mol
CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ΔH3=-58.7 kJ/mol
写出由CO与H2制备CH3OH 气体的热化学方程式____________。
(2)甲醇和CO2可直接合成碳酸二甲酯(CH3OCOOCH3简称DMC) ;
2CH3OH(g)+CO2(g) ![]() CH3OCOOCH3(g)+H2O(g) ΔH4<0
CH3OCOOCH3(g)+H2O(g) ΔH4<0
①该化学反应的平衡常数表达式为K=__________
②在恒温恒容密闭容器中发生上述反应,能说明反应达到平衡状态的是________(填编号)。
A.V正(CH3OH)= 2V逆(H2O)
B.容器内气体的密度不变
C.容器内压强不变
D.CH3OH与CO2的物质的量之比保持不变
(3)利用甲醇可制成微生物燃料电池(利用微生物将化学能直接转化成电能的装置)。某微生物燃料电池装置如图所示:
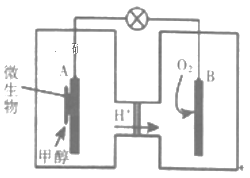
A极是_____极(填“正”或“负”),其电极反应式是_______。该电池不能在高温下工作的理由是________。
(4)一定条件下,在体积为5 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)![]() CH3OH(g)根据题意完成下列各题:
CH3OH(g)根据题意完成下列各题:
①在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=________________
②在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是_____
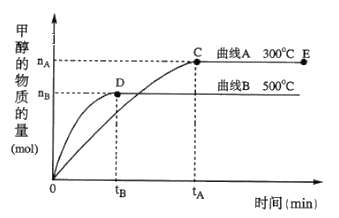
A.氢气的浓度减少
b.正反应速率加快,逆反应速率也加快
c. 甲醇的物质的量增加
d. 重新平衡时n(H2)/n(CH3OH)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组查阅资料知:苯和液溴在有溴化铁(FeBr3)存在的条件下可发生反应生成溴苯和溴化氢,此反应为放热反应。他们设计了下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A中。
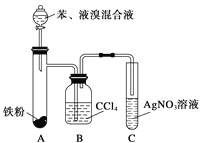
请回答下列问题:
(1)装置A中发生反应的化学方程式是______________________________。
(2)装置C中看到的现象是__________________,证明_________。
(3)装置B内盛有四氯化碳,实验中观察到的现象是_____________,原因是____。
(4)如果没有B装置,将A、C直接相连,你认为是否妥当(填“是”或“否”)________,理由是_________________________________。
(5)实验完毕后将A试管中的液体倒在装有冷水的烧杯中,烧杯____层(填“上”或“下”)为溴苯,这说明溴苯____________且____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄酒常用Na2S2O5作抗氧化剂。中华人民共和国国家标准(G112760-2011)规定葡萄酒中抗氧化剂的残留量(以游离SO2计算)不能超过0.25g/L。某化学兴趣小组制备并对SO2的化学性质和用途进行探究,探究过程实验装置如下图,并收集某葡萄酒中SO2,对其含量进行测定。(夹持仪器省略)
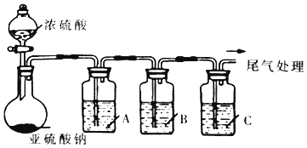
(1)实验可选用的实验试剂有浓硫酸、Na2SO3固体、Na2S溶液、BaCl2溶液、FeCl3溶液、品红溶液等.
①请完成下列表格
试剂 | 作用 | |
A | _____________ | 验证SO2的还原性 |
B | Na2S溶液 | _____________ |
C | 品红溶液 | ______________ |
②A中发生反应的离子方程式为______________________________________
(2)该小组收集某300.00mL葡萄酒中SO2,然后用0.0900 mol/L NaOH标准溶液进行滴定,滴定前排气泡时,应选择下图中的_________(填序号);若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积_____(填序号)(①= 10mL;②=40mL; ③<10mL;④>40mL)

(3)该小组在实验室中先配制0.0900 mol/L NaOH标准溶液,然后再用其进行滴定。下列操作会导致测定结果偏高的是________。
A.未用NaOH标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.配制溶液定容时,俯视刻度线
E.中和滴定时,观察标准液体积读数时,滴定前仰视,滴定后俯视
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为_______g/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,一定体积的容器中发生反应:A(s)+3B(g)![]() 2C(g)+2D(g),下列描述中能说明该反应达到平衡的是
2C(g)+2D(g),下列描述中能说明该反应达到平衡的是
①A的质量不发生变化 ②单位时间内生成a mol A,同时消耗2a mol C
③容器中的压强不再变化 ④混合气体的密度不再变化
⑤n(A)∶n(B)∶n(C)∶n(D)=1∶3∶2∶2 ⑥B的浓度不变
A. ②③⑤⑥ B. ①③④⑥ C. ②④⑤ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知自然界氧的同位素有16O、17O、18O,氢的同位素有H、D,从水分子的原子组成来看,自然界的水一共有( )
A. 3种 B. 6种 C. 9种 D. 12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应 Zn(s) +H2SO4(aq)==ZnSO4(aq) +H2(g)的反应过程如下图所示, 下列叙述中不正确的是( )
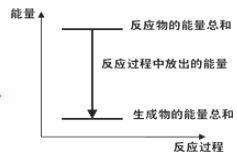
A. 若将该反应设计成原电池,正极可以是C 棒或 Fe 棒
B. 反应过程中滴加少量CuSO4 溶液可加快该反应的反应速率
C. H2SO4 的总能量大于ZnSO4 的总能量
D. 若将该反应设计成原电池,当有 32. 5g 锌溶解时,正极产生的气体在标的体积为 11. 2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X 是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。
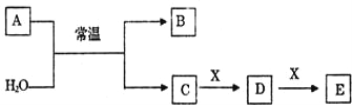
(1)若 A 为常见的金属单质,焰色反应呈黄色,X 能使品红溶液褪色,写出 C 和 E 反应的离子方程式:______________________________。
(2)若 A 为淡黄色粉末,X 为一种最常见的造成温室效应的气体。则鉴别等浓度的 D、E 两种溶液,可 选择的试剂为_____(填代号)。
A.盐酸 B.BaCl2 溶液 C.Ca(OH)2 溶液
(3)若 A 为非金属氧化物,X 是 Fe,溶液 D 中加入 KSCN 溶液变红。则 A 与 H2O 反应的化学反应方程 式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com