
【题目】工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
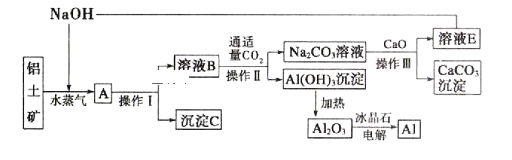
请回答下列问题。
(1)沉淀C的化学式为_______________,该物质除了用于金属冶炼以外,还可用作____________。
(2)电解熔融的氧化铝时,若得到22.4L(标准状况下)![]() ,则同时生成___________g铝。
,则同时生成___________g铝。
(3)操作I、操作II和操作III都是__________(填操作名称),实验室要洗涤,![]() 沉淀应该在____________装置中进行,洗涤方法是_____________________________。
沉淀应该在____________装置中进行,洗涤方法是_____________________________。
(4)生产过程中,除NaOH、![]() 可以循环利用外,还可以循环利用的物质有______________(填化学式),用此法制取铝的副产品是_______________(填化学式)。
可以循环利用外,还可以循环利用的物质有______________(填化学式),用此法制取铝的副产品是_______________(填化学式)。
(5)写出![]() 溶液与CaO反应的离子方程式:_________________________。
溶液与CaO反应的离子方程式:_________________________。
(6)若铝土矿中还含有二氧化硅,此生产过程中得到的氧化铝中将混有杂质_______________(填化学式)
【答案】(1)Fe2O3颜料 (2)36 (3)过滤 过滤 向漏斗中加蒸馏水至浸没沉淀,使水自然流完,重复操作2~3次
(4)CaO和CO2Fe2O3和O2
(5)CO32—+CaO+H2O===CaCO3↓+2OH-
(6)SiO2
【解析】
(1)因Al2O3+2NaOH===2NaAlO2+H2O,而Fe2O3不与NaOH溶液发生反应,因此过滤得到的沉淀C为Fe2O3,除利用Fe2O3发生铝热反应制取Fe外,还可作颜料。
(2)2Al2O3(熔融)![]() 4Al+3O2↑,n(O2)=22.4/22.4=1 mol,则m(Al)=4/3mol×27 g/mol=36 g。
4Al+3O2↑,n(O2)=22.4/22.4=1 mol,则m(Al)=4/3mol×27 g/mol=36 g。
(3)操作Ⅰ、Ⅱ、Ⅲ均是除去不溶于液体的固体,即过滤,洗涤方法是向漏斗中加蒸馏水至浸没沉淀,使水自然流完,重复操作2~3次。
(4)据流程图可看出循环使用的物质除NaOH、H2O外,还有CaCO3![]() CaO+CO2↑,CaO与CO2也可循环使用;制取Al同时得到Fe2O3和O2。
CaO+CO2↑,CaO与CO2也可循环使用;制取Al同时得到Fe2O3和O2。
(5)发生的化学反应为Na2CO3+CaO+H2O===CaCO3↓+2NaOH。
(6)据SiO2性质,SiO2+2NaOH===Na2SiO3+H2O,Na2SiO3+CO2+H2O===H2SiO3↓+Na2CO3,H2SiO3![]() SiO2+H2O,因此Al2O3中将混有SiO2。
SiO2+H2O,因此Al2O3中将混有SiO2。


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外, 曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_____。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4 蓝色溶液。
① [Ni(NH3)6]SO4中 H、N、O 元素的电负性由大到小的顺序为_____;SO42-的立体构型是_________;与 SO42-互为等电子体的微粒为_____(填化学式,任写一种)。
② 氨的沸点高于膦(PH3),原因是______; 氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为 。
(3)元素铜与镍的第二电离能分别为:ICu=1959kJ/mol ,INi=1753kJ/mol ,第二电离 ICu>INi 的原因是____________。
(4)铜的某种氯化物不仅易溶于水,而且易溶于乙醇和丙酮,其链状结构如图所示,则该氯化物的 化学式为____________________,属于_____晶体。

(5)Cu2+与乙二胺可形成上右图所示配离子,其中所含化学键类型有 ____(填标号)。
a.配位键 b.极性键 c.离子键 d.非极性键 e.金属键
(6)某镍白铜合金的立方晶胞结构如图所示。晶胞中铜原子与镍原子的数量比为_____。
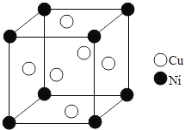
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏。“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图。已知:苯环上卤素不水解,下列有关说法不正确的是
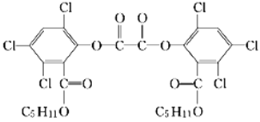
A. 草酸二酯的分子式为C26H24Cl6O8
B. 该有机物能发生加成反应、取代反应、氧化反应
C. 1 mol草酸二酯与氢气完全反应,需要氢气6 mol
D. 1 mol草酸二酯与氢氧化钠稀溶液反应,最多消耗4 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.同周期元素核电荷数越大,最外层电子数越多
B.最外层电子数越多,原子半径越小
C.从11~17号元素原子的半径逐渐增大
D.核电荷数越大,原子半径越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,溴苯是不溶于水的液体,且不与酸、碱反应,可用如图装置制取(主反应为放热反应),制取时观察到烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现。下列说法错误的是( )
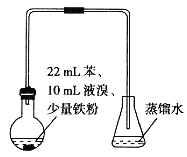
A. 制备溴苯的反应属于取代反应
B. 锥形瓶中导管口有白雾出现是因为HBr极易溶于水
C. 装置图中长玻璃导管仅起导气作用
D. 溴苯中溶有少量的溴,可用NaOH溶液除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列反应框图填空。已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应(E能引起温室效应)。
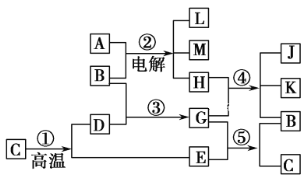
(1)单质L是________;化合物A是________。
(2)图中除反应①以外,还有两个用于工业生产的反应,是________和________(填代号)。它们反应的化学方程式分别是:____________________和_____________________。
(3)E和K、J混合溶液反应的化学方程式为_______________________________。此反应的发生说明了___________________________________________________________。
(4)把K、J混合固体放入少量浓盐酸中,则其反应的现象是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化属于吸热反应的是( )
①浓硫酸稀释 ②Ba(OH)2·8H2O与固体NH4Cl混合 ③ H2在O2中完全燃烧 ④Al与盐酸反应
A.①B.②C.③D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三届联合国环境大会的主题为“迈向零污染地球”。下列做法不应提倡的是( )
A. 推广电动汽车,践行绿色交通 B. 回收电子垃圾,集中填埋处理
C. 水果保鲜,可用浸泡过高锰酸钾溶液的硅土 D. 净化工业尾气,减少雾霾生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应NO2(g)+CO(g)=NO(g)+CO2(g)的能量变化如图所示,下列说法正确的是
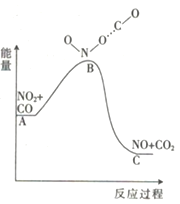
A. 图中A→B的过程为放热过程
B. 该反应为氧化还原反应
C. 1molNO2和1molCO的键能总和大于1molNO和1molCO2的键能总和
D. 1molNO2(g)和1molCO(g)的总能量低于1molNO(g)和1molCO2(g)的总能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com