
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
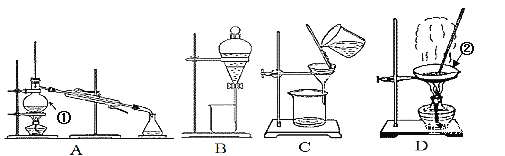
(1)装置A中仪器①的名称是______。
(2)从氯化钾溶液中得到氯化钾固体,应选择装置_____(填代表装置图的字母,下同)。
(3)分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)(已知四氯化碳和甲苯互溶),应选择装置______。
(4)从碘水中分离出I2,该装置的主要仪器名称是______,若用CCl4作为萃取剂,充分振荡后静置,观察到的现象是:______________________。
【答案】蒸馏烧瓶DA分液漏斗溶液分层,上层近乎无色,下层呈紫红色(或紫色)
【解析】
(1)装置A中仪器①的名称是蒸馏烧瓶,故答案为:蒸馏烧瓶;
(2)KCl为可溶性固体,选择蒸发分离,选择的装置为D;故答案为:D;
(3)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,可以采用蒸馏的方法,可以选择A装置,故答案为:A;
(4)从碘水中分离出I2,可以加入四氯化碳萃取剂,采用萃取的方法,选择B装置,主要仪器为分液漏斗,碘易溶于四氯化碳,且四氯化碳的密度比水大,在水的下层,可观察到下层呈紫色或紫红色,故答案为:分液漏斗;溶液分层,上层近乎无色,下层呈紫红色(或紫色)。


科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,其中W元素的原子最外层电子数是内层电子数的2倍。下列说法正确的是
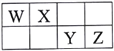
A. 原子半径大小:Z>Y>X
B. 最高价氧化物对应水化物的酸性:W>Y>Z
C. Y单质具有杀菌能力,Y与W可形成化合物WY2
D. W元素和氢元素形成的化合物可与Z单质反应,但不能与Z的氢化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
A. 常温常压下,11.2L氧气所含的原子数为NA
B. 1.8g的NH4+离子中含有的质子数为NA
C. 常温常压下,46gNO2含有的原子总数为3NA
D. 标况下,4.48LH2O中含有氢原子数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其相对分子质量为 136,分子式C8H8O2,A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环,且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如图。关于A的下列说法中不正确的是
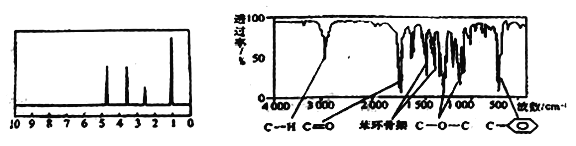
A. A分子属于酯类化合物,在一定条件下能发生水解反应
B. A在一定条件下可与3 mol H2发生加成反应
C. 符合题中A分子结构特征的有机物只有一种
D. 与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢溴酸槟榔碱是驱除动物绦虫的有效药物,可由脂A(C4H6O2)经过如下合成路线获得:

已知:Ⅰ. 含碳碳双键的有机物与氨(NH3)或胺(RNH2)反应生成新的胺类化合物
如:R1CH=CH2 + RNH2![]() R1CH2CH2NHR
R1CH2CH2NHR
Ⅱ. R1COOR2 + R3CH2COOR4![]()
![]() + R2OH
+ R2OH
请回答:
(1)化合物E的结构简式___________________。
(2)下列说法不正确的是___________________。
A. 化合物A能发生还原反应,不能发生氧化反应
B. 化合物F能与FeCl3溶液发生显色反应
C. 化合物G具有碱性,可以生成内盐
D. 氢溴酸槟榔碱的分子式为C8H14O2NBr
(3)写出B+A→C的化学方程式___________________。
(4)写出化合物B可能的同分异构体的结构简式___________________,须同时符合:
① 分子结构中有一个六元环;
② 1H-NMR谱显示分子中有3种氢原子,IR谱显示有C-N键存在。
(5)设计酯A经路径二,通过两步反应转变为化合物E的合成路线(用流程图表示,所用试剂与路径一相同)___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. HNO3的摩尔质量为63g
B. 常温、常压下,32克O2含有2NA个O
C. 标准状况下,1molH2O的体积约为22.4L
D. 1L1mol/LCH3COONa溶液中c(CH3COO—)=1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是四种常见有机物分子的比例模型示意图。下列说法正确的是( )
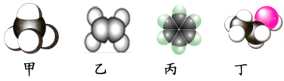
A. 甲是甲烷,甲烷能使酸性KMnO4溶液褪色
B. 乙是乙烯,乙烯可与溴水发生取代反应使溴水褪色
C. 丙是苯,苯在空气中燃烧时产生带有浓烟的火焰
D. 丁是乙酸,一定条件下乙酸能跟乙醇发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
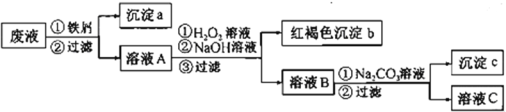
请回答:
(1)沉淀a中含有的单质是(写化学式)_______。
(2)溶液A与H2O2溶液在酸性条件下反应的离子方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过去五年,环保部向水污染、大气污染宣战,生态环境保护取得明显成效。
Ⅰ.污水中硝酸盐浓度过高,会诱发一些水体产生亚硝胺类的致癌物质。
(1)在缺氧条件下,脱氮菌(反硝化菌)以甲醇作碳源,将NO3-还原成N2的过程如下:
反硝化作用过程:NO3-![]() NO2-
NO2-![]() NO
NO![]() N2O
N2O![]() N2
N2
阶段①会生成CO2,请写出此反应的离子方程式:__________________;阶段③生成的N2O是一种强温室气体,但却可用作火箭燃料的氧化剂,,其优点是___________________。
(2)Murphy等人通过调节溶液pH为10.25,利用铝粉将NO3-转变成N2,实现化学脱氮。
要转化0.01molNO3-,需_________gAl。
Ⅱ.CO2和CH4均为温室气体,如何减少它们的排放、充分利用能源是当今社会的重要课题。
(3)二氧化碳经催化氢化可转化成绿色能源乙醇。已知:
①2H2(g)+O2(g)=2H2O(g)△H= -483.6 kJ·mol-1
②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=-1366.8kJ·mol-1
③H2O(l)=H2O(g)△H=+44.0kJ·mol-1
则二氧化碳与氢气转化成乙醇和液态水的热化学方程式为:_________。
(4)CO2和CH4在催化剂作用下可转化为合成气(CO和H2):CO2(g)+CH4(g)![]() 2CO(g)+2H2(g) △H=+247.3kJ·mol-1。向容积为1L的密闭容器中通入反应物和生成物共5.25mol,在T℃时发生反应,气体体积分数及化学反应速率与反应时间的关系如下图所示:
2CO(g)+2H2(g) △H=+247.3kJ·mol-1。向容积为1L的密闭容器中通入反应物和生成物共5.25mol,在T℃时发生反应,气体体积分数及化学反应速率与反应时间的关系如下图所示:
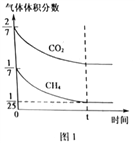
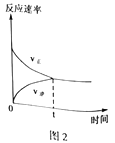
①T℃时,反应的平衡常数K=______。向平衡体系中再加入CO2、CH4、H2和CO各0.5mol,平衡将_________移动(填“向左”、“向右”或“不”)。
②写出一种既能加快化学反应速率又能提高CH4转化率的措施______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com