
【题目】某化学兴趣小组为了制取并探究氨气性质,按下列装置![]() 部分夹持装置已略去
部分夹持装置已略去![]() 进行实验。(制取氨气的反应原理:
进行实验。(制取氨气的反应原理:![]() )
)

(实验探究)
(1)A装置N元素的化合价是_______该反应是否是氧化还原反应:_______。
(2)用![]() 固体与足量
固体与足量![]() 反应,最多可制得标准状况下氨气的体积为__________L。
反应,最多可制得标准状况下氨气的体积为__________L。![]() 的摩尔质量为
的摩尔质量为![]()
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是:___________________.
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入![]() 滴浓盐酸,可观察到的现象是___________________.
滴浓盐酸,可观察到的现象是___________________.
(5)如果氨气泄漏,你应采取的急救措施是:___________________.
(6)检验氨气是否收集满的方法是__________________________________![]()
(拓展应用)
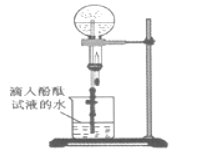
(7)某同学用下图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有_______性质![]() 填序号
填序号![]() 。
。
![]() 还原性
还原性![]() 极易溶于水
极易溶于水![]() 与水反应生成碱性物质
与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮:![]() 该反应中氨气体现_______
该反应中氨气体现_______![]() 填“氧化性”或“还原性”
填“氧化性”或“还原性”![]() 。
。
(9)请你列举出氨气的一种用途_________________________。
【答案】![]() 否
否 ![]() 氨气与水反应生成一水合氨呈碱性 产生白烟 关闭阀门,用湿毛巾捂住口鼻 用湿润的红色石蕊试纸靠近瓶口,若变蓝,则收集满
氨气与水反应生成一水合氨呈碱性 产生白烟 关闭阀门,用湿毛巾捂住口鼻 用湿润的红色石蕊试纸靠近瓶口,若变蓝,则收集满 ![]() 、C 还原性 制冷剂
、C 还原性 制冷剂
【解析】
(1)A装置为制备氨气的装置,N元素的化合价是![]() ;该反应不是氧化还原反应;
;该反应不是氧化还原反应;
(2)![]() 的物质的量
的物质的量![]() =0.1mol,由化学方程式
=0.1mol,由化学方程式![]()
![]()
![]() 可知,最多可制得
可知,最多可制得![]() 的氨气,计算标准状况下氨气的体积;
的氨气,计算标准状况下氨气的体积;
(3)干燥的氨气不能使红色石蕊试纸变色,干燥的氨气通过湿润的红色石蕊试纸,生成一水合氨,能使试纸变蓝;
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入![]() 滴浓盐酸,浓盐酸易挥发,氯化氢气体与氨气反应生成氯化铵固体,可观察到的现象是产生白烟;
滴浓盐酸,浓盐酸易挥发,氯化氢气体与氨气反应生成氯化铵固体,可观察到的现象是产生白烟;
(5)如果氨气泄漏,你应采取的急救措施是:关闭阀门,用湿毛巾捂住口鼻;
(6)检验氨气是否收集满的方法是:用湿润的红色石蕊试纸靠近瓶口,若变蓝,则收集满;
(7)烧瓶内产生红色喷泉的现象,说明氨气极易溶于水且具有碱性;
(8)由反应![]()
![]()
![]()
![]() 可分析出
可分析出![]() 作为还原剂,因此该反应中氨气体现还原性;
作为还原剂,因此该反应中氨气体现还原性;
(9)氨气可以作为制冷剂;
(1)A装置为制备氨气的装置,N元素的化合价是![]() ;该反应不是氧化还原反应,
;该反应不是氧化还原反应,
故答案为:![]() ;否;
;否;
(2)![]() 的物质的量
的物质的量![]() =0.1mol,由化学方程式
=0.1mol,由化学方程式![]()
![]()
![]() 可知,最多可制得
可知,最多可制得![]() 的氨气,标准状况下氨气的体积
的氨气,标准状况下氨气的体积![]() ,
,
故答案为:![]() ;
;
(3)干燥的氨气不能使红色石蕊试纸变色,干燥的氨气通过湿润的红色石蕊试纸,生成一水合氨,能使试纸变蓝,
故答案为:氨气与水反应生成一水合氨呈碱性;
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入![]() 滴浓盐酸,浓盐酸易挥发,氯化氢气体与氨气反应生成氯化铵固体,可观察到的现象是产生白烟,
滴浓盐酸,浓盐酸易挥发,氯化氢气体与氨气反应生成氯化铵固体,可观察到的现象是产生白烟,
故答案为:产生白烟;
(5)如果氨气泄漏,你应采取的急救措施是:关闭阀门,用湿毛巾捂住口鼻,
故答案为:关闭阀门,用湿毛巾捂住口鼻;
(6)检验氨气是否收集满的方法是:用湿润的红色石蕊试纸靠近瓶口,若变蓝,则收集满,
故答案为:用湿润的红色石蕊试纸靠近瓶口,若变蓝,则收集满;
(7)烧瓶内产生红色喷泉的现象,说明氨气极易溶于水且具有碱性,
故答案选:B、C;
(8)由反应![]()
![]()
![]()
![]() 可分析出
可分析出![]() 作为还原剂,因此该反应中氨气体现还原性,
作为还原剂,因此该反应中氨气体现还原性,
故答案为:还原性;
(9)氨气可以作为制冷剂,
故答案为:制冷剂。


科目:高中化学 来源: 题型:
【题目】(1)0.5mol·L-1MgCl2溶液中c(Cl-)为___mol·L-1,从100mL该溶液中取出20mL再稀释至100mL,c(MgCl2)为__mol·L-1。
(2)将SO2通入氯化钡溶液中无现象;若将SO2通入硝酸钡溶液中有白色沉淀产生,其化学反应方程式如下(未配平):SO2+Ba(NO3)2+H2O→BaSO4↓+HNO3+NO↑。
①配平上述化学反应方程式并用双线桥表示电子转移的方向和数目___。
②该反应中,__元素发生氧化反应,氧化剂是__(写化学式)。氧化产物与还原产物的物质的量之比为___。
③当反应消耗19.2gSO2时,反应中转移电子__mol,在标准状况下,生成NO的体积为__L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程可以达到实验目的的是( )
| 实验目的 | 实验过程 |
A. | 制取并纯化氨气 | 向浓氨水中加入生石灰,将产生的气体通过盛有 |
B. | 探究 | 向 |
C. | 比较 | 向 |
D. | 探究浓度对化学反应速率的影响 | 其他条件一定,向2支均盛有 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去)。请回答下列问题:
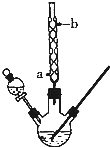
(1)水从冷凝管![]() __(填“a”或“b”)处进入。
__(填“a”或“b”)处进入。
(2)已知下列数据:
乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 | |
熔点/℃ | ﹣117.3 | 16.6 | ﹣83.6 | ﹣ |
沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
又知温度高于140℃时发生副反应:2CH3CH2OH![]() CH3CH2OCH2CH3+H2O,该副反应属于___反应(填字母)。
CH3CH2OCH2CH3+H2O,该副反应属于___反应(填字母)。
a.加成 b.取代 c.酯化 d.氧化
(3)将反应后的混合液缓缓倒入盛有足量饱和碳酸钠溶液的烧杯中,搅拌、静置。上述实验中饱和碳酸钠溶液的作用是(填字母):__。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(4)上述(3)中欲分离出乙酸乙酯,应使用的分离方法是__(填操作方法名称,下同),进行此步操作后,所得有机层中的主要无机物杂质是水,在不允许使用干燥剂的条件下,除去水可用__的方法。
(5)若实验所用乙酸质量为6.0g,乙醇质量为5.0g,得到纯净的产品质量为4.4g,则乙酸乙酯的产率是__。
(6)乙二酸和乙二醇也能发生酯化反应,写出生成环酯的化学反应方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“空气吹出法”海水提溴的工艺流程如图:
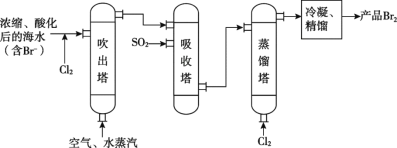
下列说法中,不正确的是( )
A.海水提溴发生的所有反应均为氧化还原反应
B.每提取1mol溴,理论上消耗氯气44.8升
C.经过吸收塔后,溴元素得到了富集
D.蒸馏塔中还发生了化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛又名香兰素,是食品和药品的重要原料,其结构简式如图所示。下列有关香草醛的说法中不正确的是( )

A.香草醛可以发生银镜反应
B.在一定条件下1mol香草醛可以与4molH2反应
C.香草醛遇FeCl3溶液可变色
D.香草醛可与NaOH溶液反应,也可与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D为由短周期元素组成的四种物质,它们有如下所示转化关系,且D为强电解质(其他相关物质可能省略)。
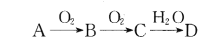
下列说法不正确的是
A. 若A为非金属单质,则它与Mg反应的产物中阴、阳离子个数比可能为2:3
B. 若A为非金属单质,则其组成元素在周期表中的位置可能处于第二周期第IVA族
C. 若A是共价化合物,则A和D有可能发生氧化还原反应
D. 若A是金属或非金属单质,则常温下0. 1 mol/L的D溶液中由水电离出的c(H+)可能为10-13mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是
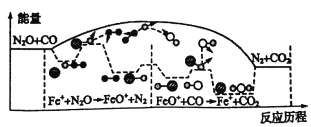
A. 反应总过程△H<0
B. Fe+使反应的活化能减小
C. 总反应若在2L的密闭容器中进行,温度越高反应速率一定越快
D. Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为放热及应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热ΔH=-3677 kJ/mol(P被氧化为P4O10),下列有关P4S3的说法不正确的是()

A. 分子中每个原子最外层均达到8电子稳定结构
B. P4S3中硫元素为-2价,磷元素为+3价
C. 一个P4S3分子中含有三个非极性共价键
D. 热化学方程式为:P4S3(s)+8O2(g)=P4O10(s)+3SO2(g) ΔH=-3677 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com