
| A. | 甲烷的二氯代物有两种 | |
| B. | 等物质的量的乙醇和乙烯完全燃烧消耗氧气的质量不同 | |
| C. | 葡萄糖能发生银镜反应,也能与氧气发生催化氧化反应 | |
| D. | 向蛋白质溶液中加入CuSO4溶液后能发生盐析 |
分析 A.甲烷为正四面体结构,四个氢原子等效;
B.根据物质的组成判断耗氧量,物质的量相同的烃CxHy的耗氧量取决于x+$\frac{y}{4}$,物质的量相同的含烃氧衍生物CxHyOz耗氧量取决于x+$\frac{y}{4}$-$\frac{z}{2}$,据此判断物质的量相同的乙烯与乙醇的耗氧量相同;
C.醛基具有还原性,能被银氨溶液氧化,发生银镜反应,醇羟基能与氧气发生催化氧化反应;
D.盐析是物理变化,硫酸铜是重金属盐,蛋白质遇重金属盐硫酸铜发生变性,属于化学变化.
解答 解:A.甲烷为空间正四面体结构,四个氢原子等效,二氯代物有1种,故A错误;
B.乙烯分子式为C2H4,其x+$\frac{y}{4}$=2+1=3,乙醇的分子式为C2H6O2,其于x+$\frac{y}{4}$-$\frac{z}{2}$=2+1.5-0.5=3,所以等物质的量的乙烯和乙醇完全燃烧时,所需氧气的量相等,故B错误;
C.葡萄糖结构简式为CH2OH(CHOH)4CHO,醇羟基能与氧气发生催化氧化反应,葡萄糖在水浴加热条件下发生银镜反应,醛基具有还原性,能被银氨溶液氧化,故C正确;
D.盐析可使蛋白质从溶液中因溶解度降低而析出,其性质不变,则可用来提纯蛋白质,硫酸铜是重金属盐,能使蛋白质发生变性,故D错误;
故选C.
点评 本题考查常见有机物的结构和性质,涉及甲烷的结构、有机物燃烧耗氧量、盐析和变性的区别等,题目难度不大,注意对课本基础知识的巩固.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去水瓶中的水垢:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O | |
| B. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| C. | 用稀氢氧化钠溶液吸收二氧化氮:2OH-+2NO2═NO3-+NO↑+H2O | |
| D. | 等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应:Ba2++2OH-+2NH4++SO42-═BaSO4↓+2NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 HCO3-+OH-,与油污发生反应,达到去污目的.
HCO3-+OH-,与油污发生反应,达到去污目的.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 建立合法、公开的地沟油回收生产制度,将生产的地沟油用作工业用油 | |
| B. | 将生活垃圾分类回收、加工、使之再生、再利用 | |
| C. | 生活污水、工业废水不要乱排放,通过打深井,将之排到地层深处 | |
| D. | 不用一次性筷子、不浪费纸张、不浪费粮食、做“光盘”一族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
 (填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式
(填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式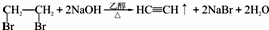 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏常用于分离提纯液态有机混合物 | |
| B. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 | |
| C. | 燃烧法是研究确定有机物成分的有效方法 | |
| D. | 核磁共振氢常用于分析有机物的相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com