
| ||
| ||
| 100�֡�87.0% |
| 87g/mol |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
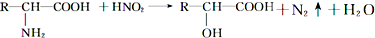 ����֪��D��E����Է��������ֱ�Ϊ162��144���ɷ�����������ת����ϵ����ͼ��ʾ��
����֪��D��E����Է��������ֱ�Ϊ162��144���ɷ�����������ת����ϵ����ͼ��ʾ��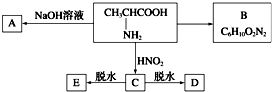
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����1����2 |
| B��n1��n2 |
| C��n1=n2 |
| D����1����2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ��� | ʵ�鷽�� | ʵ������ | ���� |
| �� | ��������Ʒ����6mLˮ���Թ�A�У������ϲ�Һ��������B��C�У� | �õ���ɫ�������ɫ��Һ | |
| �� | ��Ʒ�в���Na2SO4 | ||
| �� | ���Թ�C�У� | ��Ʒ�в���ˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
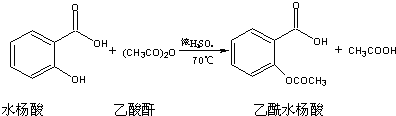
 �㷺������ʳ���У������ܾ��п����ԣ�����1mol�û�������Ӧ��Br2��H2����������ֱ�Ϊ��������
�㷺������ʳ���У������ܾ��п����ԣ�����1mol�û�������Ӧ��Br2��H2����������ֱ�Ϊ��������| A��1mol��7mol |
| B��3.5mol��7mol |
| C��3mol��6mol |
| D��6mol��7mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶ȡ� | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.5 | 2.00 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��KCl��Һ |
| B��NaOH��Һ |
| C��ϡH2SO4 |
| D��Na2SO4��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com