
【题目】关于化合物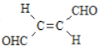 ,下列叙述正确的有( )
,下列叙述正确的有( )
A.分子间可形成氢键B.分子中既有极性键又有非极性键
C.分子中有7个![]() 键和1个
键和1个![]() 键D.C原子的杂化方式是sp2和sp3
键D.C原子的杂化方式是sp2和sp3
【答案】B
【解析】
A. 分子中形成氢键的条件为:必须同时存在氢原子和氟、氧、氮中的一种,氢原子和氟、氧、氮原子必须处在相邻的位置;
B. 共用电子对偏向一方的是极性键,没有发生偏移的是非极性键;
C. 共价单键均为![]() 键,双键中一个是
键,双键中一个是![]() 键一个是
键一个是![]() 键;
键;
D. 碳碳双键和碳氧双键均为sp2杂化;
A. 该有机物分子中含-CHO,O和H没有处于相邻的位置,不能形成氢键,A项错误;
B. C、H与C、O之间形成极性键,而C、C之间形成非极性键,则分子中既有极性键又有非极性键,B项正确;
C. 双键中含1个![]() 键和1个
键和1个![]() 键,单键均为
键,单键均为![]() 键,则分子中有9个
键,则分子中有9个![]() 键和3个
键和3个![]() 键,C项错误;
键,C项错误;
D. 分子中形成的碳碳双键和碳氧双键,杂化方式为sp2,D错误;
答案选B。


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
【题目】反应 X(g)+Y(g) ![]() 2Z(g) △H<0,在一定条件下,反应情况如图所示.若使曲线b变为曲线a可采取的措施是
2Z(g) △H<0,在一定条件下,反应情况如图所示.若使曲线b变为曲线a可采取的措施是
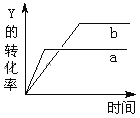
A.加入催化剂B.增大压强
C.升高温度D.保持容器体积不变,冲入He气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是( )
A. 标准状况下,11.2L的己烷所含的分子数为0.5NA
B. 28g乙烯所含共用电子对数目为4NA
C. 1mol羟基所含电子数为7 NA
D. 现有乙烯、丙烯的混合气体共14g,其原子数为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们利用原电池原理制作了多种电池,以满足日常生活、生产和科学技术等方面的需要。请根据题中提供的信息,回答下列问题。
(1)铅蓄电池在放电时的电池反应为Pb+PbO2+2H2SO4==2PbSO4+2H2O,则其正极上的电极反应为___________。
(2)FeCl3溶液腐蚀印刷电路铜板时发生反应:2FeCl3+Cu==2FeCl2+ CuCl2。若将此反应设计成原电池,则负极所用的电极材料为_____;电极反应式:_________。
(3)用Fe做阳极,KOH溶液做电解质溶液,进行电解,在阳极得到FeO![]() ,写出阳极的电极反应式____________________________________
,写出阳极的电极反应式____________________________________
(4)已知甲醇燃料电池的工作原理如下图所示。该电池工作时,b口通入的物质为_____,该电池正极上的电极反应式为 _______________;当6.4g甲醇(CH3OH)完全反应生成CO2时,有____mol电子发生转移。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数用![]() 表示,下列叙述正确的是
表示,下列叙述正确的是![]()
①![]() 含有电子数为
含有电子数为![]()
②![]() 中含有的
中含有的![]() 键总数目为
键总数目为![]()
③![]()
![]() 与
与![]() 完全反应时转移电子数为
完全反应时转移电子数为![]()
④![]() 硅晶体中含有
硅晶体中含有![]() 个
个![]() 键
键
⑤![]() 通入足量氢氧化钠溶液中充分反应,转移的电子数等于
通入足量氢氧化钠溶液中充分反应,转移的电子数等于![]()
⑥![]() ,
,![]()
![]() 溶液中,
溶液中,![]() 和
和![]() 离子数的总和是
离子数的总和是![]()
⑦在常温常压下,![]() 铁与
铁与![]()
![]() 充分反应,转移的电子数为
充分反应,转移的电子数为![]()
⑧![]() 和
和![]() 的混合物共
的混合物共![]() ,其中所含原子数一定为
,其中所含原子数一定为![]() .
.
A.①②③⑤⑧B.②④⑥⑦⑧C.①③⑤⑥⑦D.①②④⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是
A.0.1mol氧化钠固体中离子个数为0.2NA
B.1mol金刚石中含C-C键的数目为4NA
C.标准状况下,22.4L乙炔中含π键数为2NA
D.1mol NaHSO4晶体中阳离子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mn和Bi形成的晶体薄膜是一种金属间化合物![]() 晶胞结构如图
晶胞结构如图![]() ,有关说法正确的( )
,有关说法正确的( )
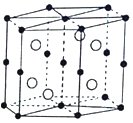
A.锰价电子排布为![]()
B.Bi是d区金属
C.该合金堆积方式是简单立方
D.该晶体的化学式为MnBi
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温常压下,N2(g)+3H2(g ) 2NH3(g) △H=-92.4 kJ /mol在同温同压下向一密闭容器中通入1molN2和3molH2,反应完后放出热量为Q1 kJ,向另一个体积相同的密闭容器通入2molNH3,相同条件下反应完成时吸收热量为Q2 kJ,且Q2=3Q1则下列说法正确的是( )
A.Q1=92.4 kJ B.Q1+Q2=92.4
C.H2的转化率为75%D.两个容器中NH3的百分含量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验结果不能作为相应定律或原理的证据之一的是( )
A | B | C | D | |
勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏加德罗定律 | |
实验方案 |
|
|
|
|
结果 | 左球气体颜色加深 右球气体颜色变浅 | 烧瓶中冒气泡 试管中出现浑浊 | 测得 |
|
(B中试剂为浓盐酸、碳酸钠溶液、硅酸钠溶液)
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com