
·ÖĪö £Ø1£©øł¾ŻøĒĖ¹¶ØĀɽ«¢Ł”Į$\frac{1}{2}$+¢ŚæɵĆĢ¼Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½£¬“Ó¶ųæÉÖŖĘäČ¼ÉÕČČ£»ĪļÖŹ¾ßÓŠÄÜĮæŌ½øߣ¬ĪļÖŹµÄĪČ¶ØŠŌŌ½Čõ£»
£Ø2£©·“Ó¦¢ŪĪŖĻ”µÄĒæĖįČÜŅŗÓėĻ”µÄĒæ¼īČÜŅŗ·“Ӧɜ³ÉŃĪŗĶĖ®µÄ·“Ó¦£»“×ĖįĪŖČõĖį£¬µēĄė¹ż³ĢŠčŅŖĪüŹÕČČĮ棬µ¼ÖĀ·ÅČČČČĮæ¼õÉŁ£¬½įŗĻģŹ±äĪŖøŗֵŊ¶Ļ£®
½ā“š ½ā£ŗ£Ø1£©¢Ł2C£Øs£©+O2£Øg£©ØT2CO£Øg£©”÷H1=-221kJ/mol
¢ŚCO£Øg£©+$\frac{1}{2}$O2£Øg£©ØTCO2£Øg£©”÷H2=-283kJ/mol
øł¾ŻøĒĖ¹¶ØĀÉ¢Ł”Į$\frac{1}{2}$+¢ŚæÉµĆ£ŗC£Øs£©+O2£Øg£©ØTCO2£Øg£©”÷H2=-393.5kJ/mol£»
øł¾Ż·“Ó¦C£Øs£¬½šøÕŹÆ£©=C£Øs£¬ŹÆÄ«£©”÷H=-1.9kJ/molæÉÖŖ£¬øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ĖµĆ÷½šøÕŹÆµÄÄÜĮæøßÓŚŹÆÄ«£¬ŌņŹÆÄ«µÄĪČ¶ØŠŌøü“ó£¬
¹Ź“š°øĪŖ£ŗ393.5kJ/mol£»ŹÆÄ«£»
£Ø2£©Ļ”ČÜŅŗÖŠH+£Øaq£©+OH-£Øaq£©ØTH2O£Øl£©”÷H3=-57.3kJ/mol±ķŹ¾Ļ”µÄĒæĖįÓėĻ”µÄĒæ¼īČÜŅŗ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£¬ČēČČ»Æѧ·½³ĢŹ½£ŗHCl£Øaq£©+NaOH£Øaq£©=H2O£Øl£©+NaCl£Øaq£©”÷H=-57.3 kJ/mol£»
Ļ”“×ĖįÓėĒāŃõ»ÆÄĘĻ”ČÜŅŗĒ”ŗĆ·“Ó¦µÄÖŠŗĶČČĪŖ”÷H4£¬ÓÉÓŚ“×ĖįµÄµēĄėĪüČČ£¬Ōņ·“Ó¦ÖŠ·Å³öČČĮæ¼õÉŁ£¬ÓÉÓŚģŹ±äĪŖøŗÖµ£¬Ōņ”÷H3£¾”÷H4£¬
¹Ź“š°øĪŖ£ŗHCl£Øaq£©+NaOH£Øaq£©=H2O£Øl£©+NaCl£Øaq£©”÷H=-57.3 kJ/mol£»”÷H3£¾”÷H4£®
µćĘĄ ±¾Ģāæ¼²éøĒĖ¹¶ØĀÉŌŚČČ»Æѧ·½³ĢŹ½ÖŠµÄ¼ĘĖć”¢ģŹ±ä±Č½ĻµČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·øĒĖ¹¶ØĀɵÄÄŚČŻ¼°Ó¦ÓĆ·½·ØĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕĪļÖŹĪČ¶ØŠŌÓė¾ßÓŠÄÜĮæµÄ¹ŲĻµ£®


 Č«ÄÜĮ·æ¼¾ķĻµĮŠ“š°ø
Č«ÄÜĮ·æ¼¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
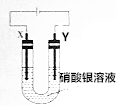 X”¢Y¾łĪŖŹÆÄ«µē¼«£¬µē½āĻõĖįŅųČÜŅŗ£¬ŹµŃé×°ÖĆČēĶ¼ĖłŹ¾£¬µē½āŹµŃé¹ż³ĢÖŠ£¬·¢ĻÖY¼«ŌöÖŲµÄĶ¬Ź±£¬Y¼«øŗ¼«²śÉśĘųÅŻĒŅĘųÅŻÓÉĪŽÉ«±äŗģ×ŲÉ«£®ŅŃÖŖµēĮ÷Š§ĀŹµČÓŚÉś³ÉÄæ±ź²śĪļĻūŗĵē×ÓŹéÓėµēĀ·×ŖŅĘ×ܵē×ÓŹżÖ®±Č£®ĻĀĮŠĶʶĻÕżČ·µÄŹĒ£Ø””””£©
X”¢Y¾łĪŖŹÆÄ«µē¼«£¬µē½āĻõĖįŅųČÜŅŗ£¬ŹµŃé×°ÖĆČēĶ¼ĖłŹ¾£¬µē½āŹµŃé¹ż³ĢÖŠ£¬·¢ĻÖY¼«ŌöÖŲµÄĶ¬Ź±£¬Y¼«øŗ¼«²śÉśĘųÅŻĒŅĘųÅŻÓÉĪŽÉ«±äŗģ×ŲÉ«£®ŅŃÖŖµēĮ÷Š§ĀŹµČÓŚÉś³ÉÄæ±ź²śĪļĻūŗĵē×ÓŹéÓėµēĀ·×ŖŅĘ×ܵē×ÓŹżÖ®±Č£®ĻĀĮŠĶʶĻÕżČ·µÄŹĒ£Ø””””£©| A£® | Y¼«ø½½ü²śÉśµÄĪŽÉ«ĘųÅŻŹĒH2 | |
| B£® | X¼«ø½½üµē½āÖŹČÜŅŗÖŠc£ØH+£©»į¼õŠ” | |
| C£® | Čō²śÉś2.24L O2£Ø±ź×¼×“æöĻĀ£©Ź±Īö³ö32.4gŅų£¬ŌņµēĮ÷Š§ĀŹĪŖ80% | |
| D£® | Ņõ¼«µÄø±·“Ó¦ĪŖNO3-+3e-+4H+ØTNO”ü+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»ÆĀĮ£ŗÖĪĮĘĪøĖį¹ż¶ąµÄŅ»ÖÖŅ©¼Į | |
| B£® | Ć÷·Æ£ŗ¾»Ė®¼Į | |
| C£® | ÉÕ¼ī£ŗÖĪĮĘĪøĖį¹ż¶ąµÄŅ»ÖÖŅ©¼Į | |
| D£® | Š”ĖÕ“ņ£ŗ·¢½Ķ·ŪÖ÷ŅŖ³É·Ö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.5mol | B£® | 1.0mol | C£® | 1.5mol | D£® | 2.0mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
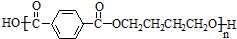
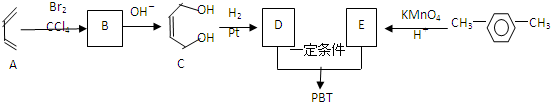
 »„ĪŖĶ¬ĻµĪļ¹ŲĻµ£®
»„ĪŖĶ¬ĻµĪļ¹ŲĻµ£®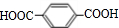 $\stackrel{Ņ»¶ØĢõ¼ž}{”ś}$
$\stackrel{Ņ»¶ØĢõ¼ž}{”ś}$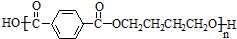 +£Ø2n-1£©H2O£®
+£Ø2n-1£©H2O£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŻĶČ”ŹĒ³£ÓƵÄÓŠ»śĪļĢį“æ·½·Ø | |
| B£® | Č¼ÉÕ·ØŹĒŃŠ¾æČ·¶ØÓŠ»śĪļ³É·ÖµÄÓŠŠ§·½·ØÖ®Ņ» | |
| C£® | ¶ŌÓŠ»śĪļ·Ö×ÓŗģĶā¹āĘ×Ķ¼µÄŃŠ¾æÓŠÖśÓŚČ·¶ØÓŠ»śĪļ·Ö×ÓÖŠµÄ¹ŁÄÜĶÅ | |
| D£® | ŗĖ“Ź²ÕńĒāĘ×Ķس£ÓĆÓŚ·ÖĪöÓŠ»śĪļµÄĻą¶Ō·Ö×ÓÖŹĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
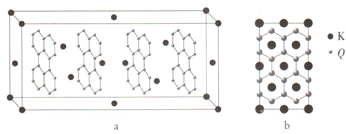 Q”¢R”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£¬QµÄŅ»ÖÖµ„ÖŹŹĒĢģČ»“ęŌŚµÄ×īÓ²µÄĪļÖŹ£¬XŌ×ÓµÄŗĖĶāµē×ÓÓŠ°ĖÖÖŌĖ¶ÆדĢ¬£¬YŌŖĖŲµÄĄė×Ó°ė¾¶ŹĒµŚČżÖÜĘŚÖŠ×īŠ”µÄ£¬ZŹĒµŚĖÄÖÜĘŚÖŠĪ“³É¶Ōµē×Ó×ī¶ąµÄŌ×Ó£®
Q”¢R”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£¬QµÄŅ»ÖÖµ„ÖŹŹĒĢģČ»“ęŌŚµÄ×īÓ²µÄĪļÖŹ£¬XŌ×ÓµÄŗĖĶāµē×ÓÓŠ°ĖÖÖŌĖ¶ÆדĢ¬£¬YŌŖĖŲµÄĄė×Ó°ė¾¶ŹĒµŚČżÖÜĘŚÖŠ×īŠ”µÄ£¬ZŹĒµŚĖÄÖÜĘŚÖŠĪ“³É¶Ōµē×Ó×ī¶ąµÄŌ×Ó£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ś¢Ü¢Ż | D£® | ¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com