
【题目】化合物F是一种非天然氨基酸,其合成路线如下:
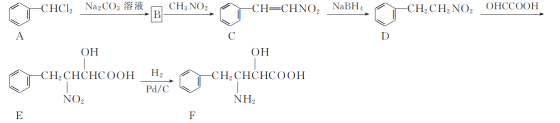
(1) C中官能团的名称为________。
(2) D→E的反应类型为________。
(3) B的分子式为C7H6O,写出B的结构简式:________。
(4) D的一种同分异构体X同时满足下列条件,写出X的结构简式: ________。
①六元环状脂肪族化合物;
②能发生银镜反应,1 mol X反应能生成4 mol Ag;
③分子中只有4种不同化学环境的氢。
(5) 写出以![]() 、CH3NO2为原料制备
、CH3NO2为原料制备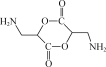 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干) _____ 。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干) _____ 。
【答案】碳碳双键、硝基 加成反应 ![]()
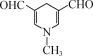 或
或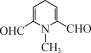 或
或![]()
【解析】
A的结构为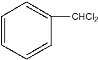 ,分子式为C7H6Cl2,不饱和度为4;B的分子式为C7H6O,不饱和度为5,因此推测B的结构为
,分子式为C7H6Cl2,不饱和度为4;B的分子式为C7H6O,不饱和度为5,因此推测B的结构为 ,即苯甲醛;C的结构为
,即苯甲醛;C的结构为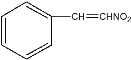 ,与NaBH4反应后生成的D的结构中不含碳碳双键,因此C发生了加成反应;由D生成E,是D与OHCCOOH反应的结果,那么根据D和E的结构推测,二者发生的是加成反应;由E生成的F结构中不再含有硝基而是代之以氨基,因此E生成F发生的是硝基还原的反应。
,与NaBH4反应后生成的D的结构中不含碳碳双键,因此C发生了加成反应;由D生成E,是D与OHCCOOH反应的结果,那么根据D和E的结构推测,二者发生的是加成反应;由E生成的F结构中不再含有硝基而是代之以氨基,因此E生成F发生的是硝基还原的反应。
(1)由C的结构可知,C中官能团的名称为碳碳双键和硝基;
(2)通过分析可知,D生成E发生的是加成反应;
(3)通过分析可知,B为苯甲醛,结构简式为: ;
;
(4)由D的结构可知,D的分子式为C8H9NO2,不饱和度为5;D的同分异构体X不含苯环,但含有六元环状结构;1mol的X可以发生银镜反应生成4mol的Ag,所以X的结构中有2个醛基;考虑到X的不饱和度也为5,所以X的结构中可能还含有两个双键,同时为了保证其分子内只有4种等效氢原子,X的结构尽可能对称;通过分析,六元环不能全由碳原子构成,这样即使结构对称也至少有5种等效氢原子,不合要求;所以可能的结构有: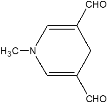 ,
,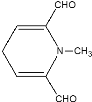 ,
, 任写一种即可;
任写一种即可;
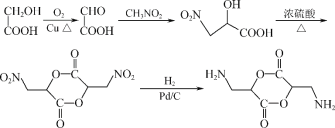
(5)由产物的结构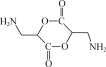 可知,其含有两个酯基,并且结构对称,所以可以认为是由两分子的同一物质相互酯化得来的;此外,由于产物结构中的氨基易被氧化,所以考虑其是在合成路线的最后一步通过硝基还原得来,那么获得产物
可知,其含有两个酯基,并且结构对称,所以可以认为是由两分子的同一物质相互酯化得来的;此外,由于产物结构中的氨基易被氧化,所以考虑其是在合成路线的最后一步通过硝基还原得来,那么获得产物 可先由2个
可先由2个![]() 发生分子之间的酯化反应,再发生硝基还原即可;那么为了获得
发生分子之间的酯化反应,再发生硝基还原即可;那么为了获得![]() 则可参照D生成E的反应,利用CH3NO2与OHCCOOH二者的加成反应获得;因此合成路线为:
则可参照D生成E的反应,利用CH3NO2与OHCCOOH二者的加成反应获得;因此合成路线为: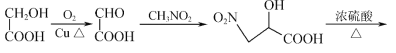
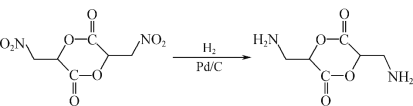 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室中用下列装置制FeCl3,可供选择的试剂有:①MnO2 ②NaOH溶液 ③饱和NaCl溶液 ④浓硫酸 ⑤浓盐酸。
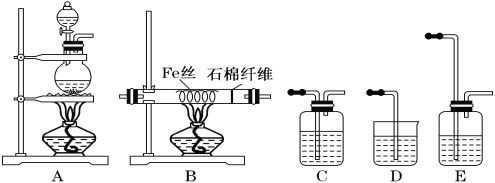
(1)按气体流向由左到右排列,各装置的连接顺序为(填写A~E序号):
_____→_______ → ______ → _____ → ______。
(2)A装置烧瓶中反应的离子方程式是______________________________________________。
(3)E中盛装的试剂是_____________,其作用是_____________________________________。
(4)停止反应后,还有铁丝剩余。为检验FeCl3的生成,并最终得到FeCl3溶液,甲同学设计以下实验步骤:
a.待B装置玻璃管冷却后,将管中物质用水溶解,_________ (填操作方法)除去不溶物;
b.取少量滤液,滴加_________________溶液,溶液呈现红色,以此检验Fe3+;
c.取少量滤液,滴加硝酸酸化的AgNO3溶液,检验Cl-。
(5)乙同学认为甲的实验设计不能最终得到FeCl3溶液,其理由是(写出相应的离子反应方程式)_____________________。
你认为还选择下列哪些试剂才能制得较为纯净的FeCl3溶液______________________。
A.KMnO4(H+) B.Fe C.H2O2 D.Cl2 E.盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.标准状况下,22.4 L水中所含的分子数约为6.02×1023个
B.1 mol Cl2中含有的原子数为NA
C.标准状况下,aL氧气和氮气的混合物含有的分子数约为![]() ×6.02×1023个
×6.02×1023个
D.常温常压下,11.2 L CO分子数是0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)2Z(g);△H<0.上图表示该反应的速率(v)随时间
(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是( )

A. ![]() 时加入了催化剂B.
时加入了催化剂B. ![]() 时降低了温度
时降低了温度
C. ![]() 时增大了压强D.
时增大了压强D. ![]() 时间内转化率最高
时间内转化率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲(52Te)被誉为“国防与尖端技术的维生素”。工业上常用铜阳极泥(主要成分是Cu2Te、含Ag、Au等杂质)为原料提取碲并回收金属,其工艺流程如下:
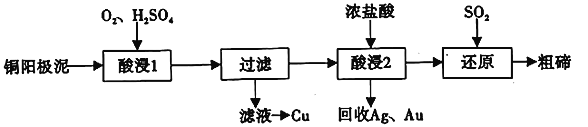
已知:TeO2微溶于水,易与较浓的强酸、强碱反应。回答下列问题:
(1)已知Te为VIA族元素,TeO2被浓NaOH溶液溶解,所生成盐的化学式为____________。
(2)“酸浸2”时温度过高会使Te的浸出率降低,原因是________________________。
(3)“酸浸1”过程中,控制溶液的酸度使Cu2Te转化为TeO2,反应的化学方程式为____________;
“还原”过程中,发生反应的离子方程式为_____________________________。
(4)工业上也可用电解法从铜阳极泥中提取碲,方法是:将铜阳极泥在空气中焙烧使碲转化为TeO2,再用NaOH溶液碱浸,以石墨为电极电解所得溶液获得Te。电解过程中阴极上发生反应的电极方程式为____________________。在阳极区溶液中检验出有TeO42-存在,生成TeO42-的原因是_____________________。
(5)常温下,向l mol·L-1 Na2TeO3溶液中滴加盐酸,当溶液pH=5时,c(TeO32-):c(H2TeO3)=__________。(已知:H2TeO3的Ka1=1.0×10-3 Ka2=2.0×10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验某溶液中是否含有![]() ,常用的方法是( )
,常用的方法是( )
A.取样,滴加BaCl2溶液,看是否有不溶于水的白色沉淀生成
B.取样,滴加稀盐酸酸化的BaCl2溶液,看是否有不落于水的白色沉淀生成
C.取样,滴加稀硫酸,再滴加BaCl2溶液,看是否有不落于水的白色沉淀生成
D.取样,滴加稀盐酸,无明显现象,再滴加BaCl2落液,看是否有不溶于水的白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量CaCl2、MgCl2、Na2SO4等杂质,实验室提供的试剂如下:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液。实验室提纯NaCl的流程如图:

(1)欲除去溶液I中的杂质,写出A所代表的多种试剂,按滴加顺序依次为I.NaOH;Ⅱ.___________;Ⅲ.____________ (填化学式)。
(2)请写出下列试剂加入时发生反应的化学方程式:
①加入试剂I: ____________________________。
②加入盐酸:______________________________________________________.
(3)操作a、b中均用到的玻璃仪器是________、_______(填仪器名称),操作c的名称为___________________。
(4)如何对操作b所得到的沉淀进行洗涤:________________________。
(5)经过操作b后,如何检验所得溶液中的SO42-已除去:______________。
(6)若上述流程中未进行操作b,即直接向溶液I中加盐酸到pH为45,过滤,得到沉淀X和溶液Y,则沉淀X为__________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色胶状沉淀,I为红褐色沉淀。(此转化关系中所用的试剂都是足量的)

(1)写出下列物质的化学式:F____________,G________________。
(2)将混合物中两种金属分离开的最简单的方法是___________。
(3)D→E的转化中,加入过量的X可能是_____________________。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______________________________________________;
H→I:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图所示。下列有关叙述正确的是( )
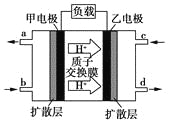
A.H+从正极区通过交换膜移向负极区
B.负极的电极反应式为:CH3OH(l)+H2O(l)-6e-===CO2(g)+6H+
C.d导出的是CO2
D.图中b、c加入的分别是O2、甲醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com