
【题目】元素周期表中第三周期包括Na、Mg、Al、Si、P、S、Cl、Ar 8种元素。请回答下列问题:
(1)基态磷原子核外有________种运动状态不同的电子。
(2)第三周期8种元素按单质熔点(℃)大小顺序绘制的柱形图(已知柱形“1”代表Ar)如下所示,则其中“2”原子的结构示意图为________,“8”单质晶体的类型为________。


(3)氢化镁
储氢材料的晶胞结构如图所示,已知该晶体的密度为ρ g·cm-3,则该晶体的化学式为________,晶胞的体积为________cm3(用ρ、NA表示,其中NA表示阿伏加德罗常数的值)。
(4)实验证明:KCl、MgO、CaO三种晶体的结构与NaCl晶体的结构相似,已知NaCl、KCl、CaO晶体的晶格能数据如下表:
晶体 | NaCl | KCl | CaO |
晶格能/(kJ·mol-1) | 786 | 715 | 3 401 |
则KCl、MgO、CaO三种晶体的熔点从高到低的顺序是________________。其中MgO晶体中一个Mg2+周围和它最近且等距离的Mg2+有________个。
(5)Si、C和O的成键情况如下:
化学键 | C-O | C=O | Si-O | Si=O |
键能/(kJ·mol-1) | 360 | 803 | 464 | 640 |
C和O之间易形成含有双键的CO2分子晶体,而Si和O之间则易形成含有单键的SiO2原子晶体,请结合数据分析其原因:__________________________________________。
【答案】 15 ![]() 原子晶体 MgH2 52/(ρNA) MgO>CaO>KCl 12 碳与氧之间形成含有双键的分子放出的能量(2×803 kJmol-1=1606 kJmol-1)大于形成含单键的原子晶体放出的能量(4×360 kJmol-1=1440 kJmol-1),故碳与氧之间易形成含双键的CO2分子晶体;硅与氧之间形成含有双键的分子放出的能量(2×640 kJmol-1=1280 kJmol-1)小于形成含单键的原子晶体放出的能量(4×464 kJmol-1=1856 kJmol-1),故硅与氧之间易形成含单键的SiO2原子晶体
原子晶体 MgH2 52/(ρNA) MgO>CaO>KCl 12 碳与氧之间形成含有双键的分子放出的能量(2×803 kJmol-1=1606 kJmol-1)大于形成含单键的原子晶体放出的能量(4×360 kJmol-1=1440 kJmol-1),故碳与氧之间易形成含双键的CO2分子晶体;硅与氧之间形成含有双键的分子放出的能量(2×640 kJmol-1=1280 kJmol-1)小于形成含单键的原子晶体放出的能量(4×464 kJmol-1=1856 kJmol-1),故硅与氧之间易形成含单键的SiO2原子晶体
【解析】(1)磷原子核电荷数为15,电子排布为1s22s22p63s23p3,每个电子的运动状态不同,因此基态磷原子核外有15种运动状态不同的电子;正确答案:15。
(2)第三周期8种元素按单质算,排出氩气外,只有氯气为气体,熔点较低,氯原子核电荷数为17,原子的结构示意图为:![]() ;单质硅为原子晶体,熔点最高;正确答案:
;单质硅为原子晶体,熔点最高;正确答案:![]() ;原子晶体。
;原子晶体。
(3)根据晶胞结构可知,该晶胞中含有镁原子个数为8×1/8+1=2, 含有氢原子个数为4×1/2+2=4,镁原子与氢原子个数比为1:2,所以氢化镁化学式为MgH2;该晶胞中含有2个MgH2,则该晶胞的体积为2×26/ρNA= 52/(ρNA)cm3;正确答案:MgH2;52/(ρNA)。
(4) 晶格能越大,离子晶体熔点就越高,而晶格能大小与离子的电荷和半径有关,电荷越多,离子半径越小,晶格能就越大;KCl、MgO、CaO这3种晶体的结构与NaCl晶体结构相似,MgO、CaO中离子都带2个单位电荷,KCl中离子都带1个单位电荷,离子半径Cl->O2-,Mg2+<Ca2+<K+,高价化合物的晶格能远大于低价离子化合物的晶格能,晶格能MgO>CaO>KCl ,故熔点MgO>CaO>KCl;在MgO晶胞中Mg2+周围有六个O2-,O2-周围有六个Mg2+,根据晶胞的结构可以看出,如果以体心上一个Mg2+为究对象,和它最邻近且等距离的Mg2+分布在晶胞每个棱边中点上,共有12个;正确答案:MgO>CaO>KCl;12。
(5) C和O之间易形成含有双键的CO2分子晶体,而Si和O之间则易形成含有单键的SiO2原子晶体,其原因: 碳与氧之间形成含有双键的分子放出的能量(2×803 kJmol-1=1606 kJmol-1)大于形成含单键的原子晶体放出的能量(4×360 kJmol-1=1440 kJmol-1),故碳与氧之间易形成含双键的CO2分子晶体;硅与氧之间形成含有双键的分子放出的能量(2×640 kJmol-1=1280 kJmol-1)小于形成含单键的原子晶体放出的能量(4×464 kJmol-1=1856 kJmol-1),故硅与氧之间易形成含单键的SiO2原子晶体;正确答案:碳与氧之间形成含有双键的分子放出的能量(2×803 kJmol-1=1606 kJmol-1)大于形成含单键的原子晶体放出的能量(4×360 kJmol-1=1440 kJmol-1),故碳与氧之间易形成含双键的CO2分子晶体;硅与氧之间形成含有双键的分子放出的能量(2×640 kJmol-1=1280 kJmol-1)小于形成含单键的原子晶体放出的能量(4×464 kJmol-1=1856 kJmol-1),故硅与氧之间易形成含单键的SiO2原子晶体。


科目:高中化学 来源: 题型:
【题目】研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验:
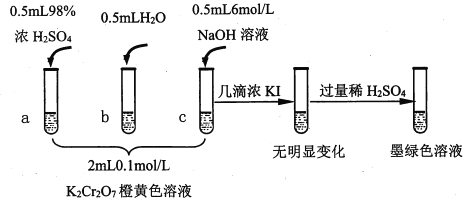
已知:Cr2O72- (橙色)+H2O![]() 2CrO42-(黄色)+2H+ △H= +13.8 kJ/mol,+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
2CrO42-(黄色)+2H+ △H= +13.8 kJ/mol,+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
(1)试管c和b对比,推测试管c的现象是________。
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?____(“是”或“否”),理由是_________________________________。
(3)对比试管a、b、c的实验现象,得到的结论是________________。
(4)试管c继续滴加KI溶液、过量稀H2SO4,分析上图的实验现象,得出的结论是_______;写出此过程中氧化还原反应的离子方程式________________。
(5)小组同学用电解法处理含Cr2O72-废水,探究不同因素对含Cr2O72-废水处理的影响,结果如下表所示(Cr2O72-的起始浓度,体积、电压、电解时间均相同)。
实验 | ⅰ | ⅱ | ⅲ | ⅳ |
是否加入Fe2(SO4)3 | 否 | 否 | 加入5g | 否 |
是否加入H2SO4 | 否 | 加入1mL | 加入1mL | 加入1mL |
电极材料 | 阴、阳极均为石墨 | 阴、阳极均为石墨 | 阴、阳极均为石墨 | 阴极为石墨,阳极为铁 |
Cr2O72-的去除率/% | 0.922 | 12.7 | 20.8 | 57.3 |
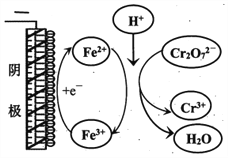
①实验ⅱ中Cr2O72-放电的电极反应式是________________。
②实验ⅲ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使一镁铝合金粉末在过量稀H2SO4中溶解,在所得溶液中加入NaOH溶液,生成沉淀的质量W和加入NaOH溶液的体积V的关系如图所示,则该合金中镁和铝的物质的量之比为

A. 1∶1 B. 2∶3 C. 8∶9 D. 4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气用于自来水的杀菌消毒,但在消毒时会产生一些负面影响,因此人们开始研究一些新型自来水消毒剂。某学习小组查阅资料发现NCl3可作为杀菌消毒剂,该小组利用如图所示的装置制备NCl3,并探究NCl3的漂白性。NCl3的相关性质如下:
物理性质 | 制备原理 | 化学性质 |
黄色油状液体,熔点为-40 ℃,沸点为 71 ℃,不溶于冷水,易溶于有机溶剂,密度为 1.65 g·mL-1 | Cl2与NH4Cl水溶液在低温下反应 | 95 ℃ 爆炸,热水中发生水解 |

回答下列问题:
(1)根据实验目的,接口连接的顺序为1-________-________-2-3-6-7-________-________-____。
(2)C装置中盛放的试剂为饱和食盐水,E装置中盛放的试剂为____________________。
(3)A装置中发生反应的离子方程式为_________________________________________。
(4)B装置中发生反应的化学方程式为___________________________________,当B装置蒸馏烧瓶中出现较多油状液体后,关闭接口2处的活塞,控制水浴加热的温度为 __________________。
(5)当E装置的锥形瓶内有黄色油状液体出现时,用干燥、洁净的玻璃棒蘸取该液体滴到干燥的红色石蕊试纸上,不褪色;若取该液体滴入热水中,片刻后取该热水再滴到干燥的红色石蕊试纸上,先变蓝后褪色,结合反应方程式解释该现象: _____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3②NO2进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度为( )
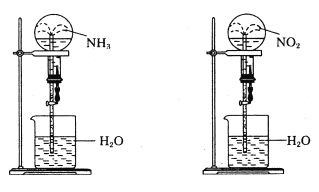
A. ①>② B. ①<② C. ①=② D. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为元素周期表中前四周期元素,原子序数依次增大,A元素原子核外有3个未成对电子,B元素原子核外电子占用3个能级,其中最高能级上的电子数是其所在能层数的2倍,D元素与B元素同族,C元素与A元素同族,E元素的负一价离子的最外层电子数与次外层的相同。F元素原子的价电子数比其余电子数少8。
(1)A、C、D的第一电离能由大到小的顺序为_____________(用元素符号表示),F在元素周期表中的位置__________。
(2)B、D形成的化合物中属于非极性分子的是_______(填化学式)。
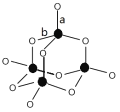
(3)B、C形成的某种化合物结构如图所示,该结构中C-B键的键长有两类,键长较短的键为_______________(填图中字母a或b),1mol该分子中含有的σ键数目为________。C、E形成某化合物,其分子中所有原子的最外层均为8电子稳定结构,该化合物的电子式为________。
(4)元素E的含氧酸中,酸性最强的是________(写化学式),该酸根离子的立体构型为________。
(5)F可与CO形成羰基配合物F2(CO)8,橘红色固体,是有机合成的重要催化剂,可用作汽油抗震剂等,不溶于水,溶于乙醇、乙醚、苯,熔点50~51℃,45℃(1.33kPa)时升华。
①F2(CO)8为_________晶体(填晶体类型)。
②F2(CO)8晶体中存在的作用力有_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期原子序数依次增大的元素A、B、C、D、E中,A的基态原子核外3个能级上有电子,且每个能级上的电子数相等,B原子核外电子有7种不同的运动状态,C元素原子核外的M层中只有2对成对电子,D+与C2-的电子数相等,E元素位于元素周期表的ds区,且基态原子价电层电子均已成对。
回答下列问题:
(1)E2+的外围电子排布图为________________。
(2)五种元素中电负性最小的是________(填元素符号),CAB-离子中,A原子的杂化方式是________。
(3)AB-、D+和E2+三种离子组成的化学物质D2E(AB)4,该化合物中存在一个复杂离子,该离子的化学式为________,配位体是________。
(4)C和E两种元素组成的一种化合物的晶胞如图所示。
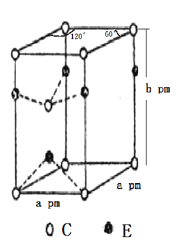
①该化合物的化学式为________,E的配位数为________,C采取________(填“简单立方”、“体心立方”、“六方最密”或“面心立方最密”)堆积;
②列式表示该晶体的密度:________g·cm-3。(NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O。取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O。取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
请回答下列问题:
(1)参加反应的二氧化锰的质量为____________。
(2)反应中被氧化的HCl的物质的量为 ____________。
(3)实验室备用的浓盐酸质量分数为36.5%,密度为1.19g·cm-3,请计算出该浓盐酸的物质的量浓度______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】榴石矿石可以看作CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下:
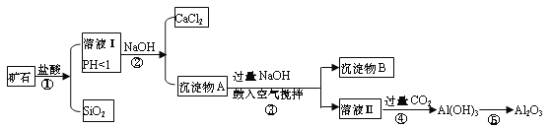
(1)用方程式表示盛放氢氧化钠溶液的试剂瓶不能用玻璃塞的原因________;
(2)溶液Ⅰ中除了Ca2+外,还可能含有的金属阳离子有_______________;
(3)步骤③中NaOH参加反应的离子方程式是________________,鼓入空气并充分搅拌的目的是_____________________。
(4)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是___________;写出步骤④通入过量CO2的离子方程式 _________________________________。
(5)试设计实验证明榴石矿中含有FeO(试剂任选,说明实验操作与现象)_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com