
【题目】有下列几种反应类型:①消去、②加聚、③水解、④加成、⑤还原、⑥氧化。用丙醛制取1,2-丙二醇,按正确的合成路线依次发生的反应所属类型应是
A. ⑤①④③ B. ⑥④③① C. ①②③⑤ D. ⑤③④①
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】MgSO4·7H2O在医药上常用做泻药,工业上可用氯碱工业中的一次盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸和碳酸盐等成分。其主要工艺如下:

请回答下列问题:
(1)用H2SO4调节溶液pH至l~2,H2SO4作用是___________________;
(2)加NaClO溶液至pH=5~6并加热煮沸5~10分钟,沉淀2中主要含有MnO2和另外两种难溶物,这两种难溶物的化学式分别为____________________、____________________;
其中NaClO溶液将MnSO4转化为MnO2的离子方程式为______________________________。
(3)检验滤液II中是否含有Fe3+的实验方法是____________________。
(4)将制得的样品5g溶于200mL水,加入2mol·L-1的盐酸5mL,在不断搅拌下滴加足量2mol·L-1BaCl2溶液,充分反应后,得沉淀4.46g,则样品纯度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“摩尔盐”是分析化学中的重要试剂,化学式为(NH4)2Fe(SO4)2·6H2O。“摩尔盐”在一定条件下分解的方程式为:4[(NH4)2Fe(SO4)2·6H2O] ![]() 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
(1)铁元素在元素周期表中的位置为________,其价层电子排布图为________。
(2)组成“摩尔盐”的非金属元素中第一电离能最大的元素为________。“摩尔盐”的分解产物中属于非极性分子的化合物是________。
(3)NH3的沸点比N2O的沸点________(填“高”或“低”),其主要原因是________。
(4)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中除了离子键以外还存在的化学键为________,与CN—互为等电子体的单质的分子式为_________。HCN分子中σ键和π键的个数之比为________。
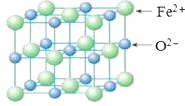
(5)FeO晶胞结构如下图所示,FeO晶体中Fe2+配位数为________,若该晶胞边长为acm,则该晶胞密度为________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关基本营养物质说法正确的是
A.淀粉和纤维素互为同分异构体
B.油脂没有固定的熔沸点
C.葡萄糖、果糖、蔗糖都能发生水解反应
D.糖类、油脂、蛋白质都是高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼是一种重要的化工原料。某同学设计的三氯化硼制备装置如下图:

【查阅资料】
①BCl3的熔点为―107.3 ℃,沸点为12.5 ℃
②2B+6HCl![]() 2 BCl3+3H2
2 BCl3+3H2
请回答下列问题:
(1)A装置可用高锰酸钾固体与浓盐酸反应制氯气,反应的化学方程式为________。
(2)为了完成三氯化硼的制备,装置从左到右的接口连接顺序为:_______________
a→(___,___)→(___,___) →(___,___)→(___,___)→j。
(3)装置E中的试剂为_______,如果拆去E装置,可能的后果是 _____________。
(4)D装置中发生反应前先通入一段时间的氯气,其目的是__________,该装置中发生反应的化学方程式为 _________________________。
(5)三氯化硼与水能剧烈反应生成两种酸,写出该反应的化学方程式 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 凡能发生银镜反应的有机物一定是醛
B. 在氧气中燃烧时只生成CO2和H2O的物质一定是烃
C. 苯酚有弱酸性,俗称石炭酸,因此它是一种羧酸
D. 用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 .
(2)烧杯间填满碎泡沫塑料的作用是 .
(3)理论上稀的强酸溶液与强碱溶液反应生成1mol水时放出57.3kJ的热量,写出表示稀盐酸和稀氢氧化钠溶液反应的中和热的热化学方程式:
(4)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大”、“偏小”或“无影响”).
(5)实验中改用60mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”),所求中和热(填“相等”或“不相等”),简述理由: .
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会(填“偏大”“偏小”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.物质的量就是1摩尔物质的质量
B.1 mol过氧化氢中含有2 mol氢和2 mol氧
C.1 mol H2中含有6.02个氢分子
D.NH3的摩尔质量是17 g· mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com