
| A. | 凡含有食品添加剂的食物对人体健康均有害 | |
| B. | 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱 | |
| C. | 施肥时,农家肥草木灰(有效成分K2CO3)不能与氮肥NH4Cl混合使用 | |
| D. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
分析 A.合理使用食品添加剂,对丰富食品生产和促进人体健康有好处;
B.钙离子与肥皂可生成高级脂肪酸钙沉淀;
C.铵态氮肥和碱性物质可以反应,且能生成氨气,从而降低肥效;
D.防氧化就是防止氧气的进入并与之反应,防受潮就是防止水分的进入.
解答 解:A.食品添加剂可以改善食品的色香味、延长食品的保质期,可适量添加使用,不能过量,故A错误;
B.含钙离子浓度较大的地下水与高级脂肪酸钠反应可生成高级脂肪酸钙沉淀,去污能力减弱,故B正确;
C.施肥时,农家肥草木灰(有效成分K2CO3)能与氮肥NH4Cl反应生成氨气,从而降低肥效,故C正确;
D.在食品袋中放入盛有硅胶和铁粉的透气小袋,硅胶(具有吸湿性)能吸收水分,铁是较活泼的金属,具有还原性,能防止食品被氧化,故D正确.
故选A.
点评 本题考查了物质的性质与用途,把握常见物质的性质与用途的关系是解答的关键,侧重化学与生活、生产的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 分液、蒸馏、萃取 | C. | 萃取、蒸馏、分液 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60能溶于二硫化碳中形成无色透明的溶液,可以用相似相溶原理解释 | |
| B. | 向含有Fe2+的溶液中滴加无色的铁氰化钾溶液,可以观察到蓝色沉淀产生 | |
| C. | 甲烷是空间正四面体结构,四个氢的相对位置完全等效,其任意取代物都不会产生同分异构现象 | |
| D. | 电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
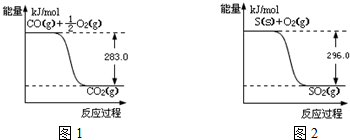
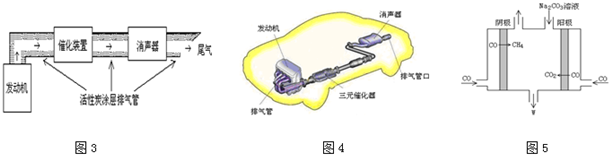
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
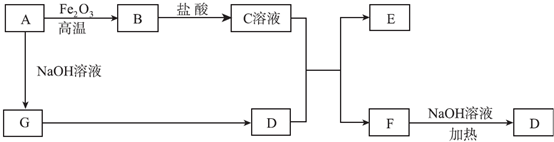
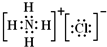 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 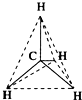 结构示意图 | B. |  电子式 | C. | 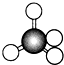 球棍模型 | D. | 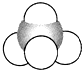 比例模型 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com