
���� ��1��ԭ��ط�Ӧ�������Է����еķ��ȵ�������ԭ��Ӧ��
��2��ԭ��ص�ط�Ӧ�У�ʧ���ӻ��ϼ����ߵĽ������������õ��ӻ��ϼ۽��͵ĵ����Ϊ��ԭ����е���ʣ�������ʧ���ӷ���������Ӧ�������ϵõ��ӷ�����ԭ��Ӧ��
��3��ʧ���ӻ��ϼ����ߵķ�Ӧ���������Ӧ��
��� �⣺��1��A��B�з�Ӧǰ���Ԫ�ػ��ϼ۲��䣬���Բ�����������ԭ��Ӧ��C����Ԫ�ػ��ϼ������������е���ת�ƣ�����Ƴ�ԭ��أ���ѡC��
��2��C��CuԪ�ػ��ϼ���0�۱�Ϊ+2�ۡ�FeԪ�ػ��ϼ���+3�۱�Ϊ+2�ۣ�����Cu����������Ӧ���������缫��ӦʽΪCu-2e-=Cu2+���Ȼ����õ��ӷ�����ԭ��Ӧ�������Ȼ�����ҺΪ�������Һ������Cu-2e-=Cu2+��������ת�Ƶ���0.6mol��������0.3mol��ͭ������Ϊ��0.3mol��64g/mol=19.2g���ʴ�Ϊ��Cu-2e-=Cu2+���Ȼ�����Һ��19.2g��
��3��ʧ���ӻ��ϼ����ߵķ�Ӧ���������Ӧ����������Ӧ��NO2ת��ΪNO3-��������Ի�����֪�÷�Ӧ��������ӦΪ2NO2-2e-+H2O�T2H++2NO3-���ʴ�Ϊ��2NO2-2e-+H2O�T2H++2NO3-��
���� ���⿼����ԭ�����Ƽ�ԭ��ط�Ӧ�ص㣬���ݵ�ط�ӦʽԪ�ػ��ϼ�����ȷ�����������������Һ��һ����˵�����ϼ����ߵĽ������������������ϼ����ߵĵ����Ϊԭ��ص���ʣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
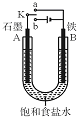 ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 CH3COOC2H5+H2O��
CH3COOC2H5+H2O��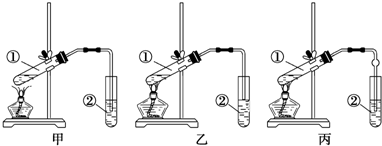
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHCO3��Һ | B�� | KSCN��Һ | C�� | NaOH��Һ | D�� | NH3•H2O��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
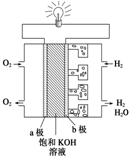 I����Դ�������������ᷢչ�Ļ��������������������Դ��̫���ܣ�����Ȼ������һ��Դ��ɹ�����ֲ��Ĺ�����ã����������ǿ����������ɫ��Դ����֪��������ֵ��143kJ•g-1����ֵָ������һ�������µ�λ������������ȫȼ�����ų�������������ת��ΪҺ̬ˮ������д������ȼ�յ��Ȼ�ѧ����ʽH2��g��+$\frac{1}{2}$O2��g��=H2O��1������H=-286kJ•mol-1��2H2��g��+O2��g��=2H2O��l����H=-572KJ•mol-1��
I����Դ�������������ᷢչ�Ļ��������������������Դ��̫���ܣ�����Ȼ������һ��Դ��ɹ�����ֲ��Ĺ�����ã����������ǿ����������ɫ��Դ����֪��������ֵ��143kJ•g-1����ֵָ������һ�������µ�λ������������ȫȼ�����ų�������������ת��ΪҺ̬ˮ������д������ȼ�յ��Ȼ�ѧ����ʽH2��g��+$\frac{1}{2}$O2��g��=H2O��1������H=-286kJ•mol-1��2H2��g��+O2��g��=2H2O��l����H=-572KJ•mol-1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2ͨ�������ˮ�У�SO2+NH3•H2O=NH4++HSO3- | |
| B�� | ��CH3COO��2Ba��Һ�е���ϡ���Ba2++SO42-=BaSO4�� | |
| C�� | ��Ag���缫�����AgNO3��Һ��4Ag++2H2O=4Ag��+O2��+4H+ | |
| D�� | AgCl����Һ�м���Na2S��Һ��2AgCl+S2-=Ag2S+2Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȩ���Ľṹ��ʽ-COH | B�� | ������ӵı���ģ��Ϊ��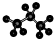 | ||
| C�� | ���Ȼ�̼���ӵĵ���ʽΪ 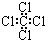 | D�� | 2-�һ�-1��3-����ϩ�ļ���ʽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4 | B�� | CO | C�� | CO2 | D�� | SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.5 mol | B�� | 0.6 mol | C�� | 0.7 mol | D�� | 0.8 mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com