
½ńÓŠČēĻĀČżøöČČ»Æѧ·½³ĢŹ½£ŗ
![]() H2£Øg£©+ 1/2 O2(g)
H2£Øg£©+ 1/2 O2(g) ![]() H2O(g) £» ”÷H£½a kJ/mol
H2O(g) £» ”÷H£½a kJ/mol
H2£Øg£©+ 1/2 O2(g) ![]() H2O(l) £» ”÷H£½b kJ/mol
H2O(l) £» ”÷H£½b kJ/mol
2 H2£Øg£©+ O2(g) ![]() 2 H2O(l) £» ”÷H£½c kJ/mol
2 H2O(l) £» ”÷H£½c kJ/mol
ĻĀĮŠ¹ŲÓŚĖüĆĒµÄ±ķŹöÕżČ·µÄŹĒ
A£®ĖüĆĒ¶¼ŹĒĪüČČ·“Ó¦ B£® a”¢bŗĶc¾łĪŖÕżÖµ
C£®·“Ó¦ČČµÄ¹ŲĻµ£ŗa=b D£®·“Ó¦ČČµÄ¹ŲĻµ£ŗ2b=c

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 H2O£Øg£©£»”÷H=a kJ/mol
H2O£Øg£©£»”÷H=a kJ/mol H2O£Øl£©£»”÷H=b kJ/mol
H2O£Øl£©£»”÷H=b kJ/mol 2H2O£Øl£©£»”÷H=c kJ/mol£®
2H2O£Øl£©£»”÷H=c kJ/mol£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| 1 |
| 2 |
| 1 |
| 2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
(1)H2(g)+![]() O2(g)
O2(g) ![]() H2O(g)””¦¤H1=a kJ”¤mol-1??
H2O(g)””¦¤H1=a kJ”¤mol-1??
(2)H2(g)+![]() O2(g)
O2(g) ![]() H2O(l)””¦¤H2=b kJ”¤mol-1??
H2O(l)””¦¤H2=b kJ”¤mol-1??
(3)2H2(g)+O2(g) ![]() 2H2O(l)””¦¤H3=c kJ”¤mol-1??
2H2O(l)””¦¤H3=c kJ”¤mol-1??
ĻĀĮŠ¹ŲÓŚĖüĆĒµÄ±ķŹöÕżČ·µÄŹĒ£Ø””””£©?
A.ĖüĆĒ¶¼ŹĒĪüČČ·“Ó¦ B.a”¢bŗĶc¾łĪŖÕżÖµ?
C.a=b£¼0? D.2b=c£¼0??
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A.Čżøö¶¼ŹĒĪüČČ·“Ó¦ B.a”¢b”¢c¾łĪŖÕżÖµ
C.a=b D.2b=c
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2010”Ŗ2011ѧğ¹ć¶«Ź”¹ćÖŻĮłÖŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ĒāĘųŹĒČĖĄą×īĄķĻėµÄÄÜŌ“”£ŅŃÖŖŌŚ25”ę”¢101kPaĻĀ£¬1 gĒāĘųĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®Ź±·Å³öČČĮæ142.9kJ£¬½ńÓŠČēĻĀČżøöČČ»Æѧ·½³ĢŹ½£ŗ
(1)H2(g)+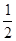 O2(g) £½ H2O(g)””¦¤H1£½a kJ”¤mol-1
O2(g) £½ H2O(g)””¦¤H1£½a kJ”¤mol-1
(2)H2O(l) £½ H2(g)+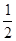 O2(g) ¦¤H2£½b kJ”¤mol-1
O2(g) ¦¤H2£½b kJ”¤mol-1
(3)2H2(g)+O2(g) £½ 2H2O(l)””¦¤H3£½c kJ”¤mol-1
ĻĀĮŠ¹ŲÓŚĖüĆĒµÄ±ķŹöÕżČ·µÄŹĒ
| A£®2b£½c | B£®b£½285.8 |
| C£®a£½£b? | D£®ĒāĘųµÄČ¼ÉÕČČĪŖa kJ”¤mol-1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com