
【题目】在一定温度下,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )
A. 单位时间内生成nmolA2同时生成nmolAB
B. 单位时间内生成2nmolAB的同时生成nmolB2
C. 容器内的总物质的量不随时间变化
D. 单位时间内断开1molA-A键的同时生成2molA-B键
【答案】B
【解析】分析:A项,单位时间内生成nmolA2同时生成nmolAB,逆反应速率大于正反应速率,反应逆向移动;B项,单位时间内生成2nmolAB的同时生成nmolB2,说明正逆反应速率相等,反应平衡;C项,该反应方程式左右两边气体分子数不变,整个反应过程容器内总物质的量都不随时间变化;D项,整个反应过程中单位时间内断开1molA-A键的同时生成2molA-B键,均表示正反应速率,无法判断是否达到平衡状态。
A项,单位时间内生成nmolA2同时生成nmolAB,逆反应速率大于正反应速率,反应逆向移动,故A项错误;
B项,单位时间内生成2nmolAB的同时生成nmolB2,说明正逆反应速率相等,反应平衡,故B项正确;
C项,该反应方程式左右两边气体分子数不变,整个反应过程容器内总物质的量都不随时间变化,故C项错误;
D项,整个反应过程中单位时间内断开1molA-A键的同时生成2molA-B键,均表示正反应速率,无法判断是否达到平衡状态,故D项错误。
综上所述,本题正确答案为B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下进行反应:mA(g)+nB(g)pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,v正、v逆随时间变化过程均如图所示,下列有关叙述正确的是( )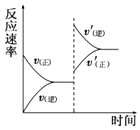
A.正反应是吸热反应,m+n>p+q
B.逆反应是吸热反应,m+n<p+q
C.正反应是吸热反应,m+n<p+q
D.逆反应是吸热反应,m+n>p+q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
①消毒 ②维持水分代谢平衡 ③维持无机盐代谢的平衡 ④降温
⑤是细胞的等渗溶液并有清洁作用
A. ①②④ B. ③②⑤ C. ②⑤③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B两种液态有机物均由碳、氢、氧三种元素组成。A能溶于水,它的相对分子质量是60,分子中有8个原子,其中氧原子数与碳原子数相等,且A与碳酸钠溶液混合时冒气泡。B分子中有9个原子,分子内所有原子的核电荷数之和为26,且B只能跟钠反应放出氢气,不能与碳酸钠溶液反应。
(1)A的结构简式为 __________________ ,B的结构简式为 ________________。
(2)写出A与碳酸钠溶液反应的化学方程式________________________________。
(3)写出B与钠反应的化学方程式_____________________________。
(4)写出A与B反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO47H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量.实验步骤如下: 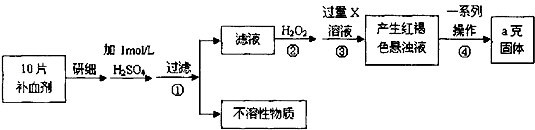
请回答下列问题:
(1)步骤②加入过量H2O2的目的: .
(2)步骤③中反应的离子方程式: .
(3)步骤④中一系列处理的操作步骤:过滤、、灼烧、冷却、称量.
(4)若实验无损耗,则每片补血剂含铁元素的质量g.
(5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定.(5Fe2++MnO4﹣+8H+═5Fe3++Mn2++4H2O) ①上述实验中的KMnO4溶液需要酸化,用于酸化的酸是 .
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硝酸
②滴定到终点时(恰好完全反应)的颜色为色.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。
B | C | D | ||
A | E |
请用化学用语回答下列问题:
(1)A、D、E元素简单离子半径由大到小的顺序为 > > (填粒子符号)_____
(2)F与D同主族且相邻二者气态氢化物稳定性的大小关系为 > (填粒子符号)_________
(3)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放出一个电子,同时产生一种
具有较强氧化性的阳离子,试写出该阳离子的电子式:______________。该阳离子中存在的化学键有_________。
(4)由C、E两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子中C、E两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。写出甲遇水蒸气的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种香料,可用下图的设计方案合成。
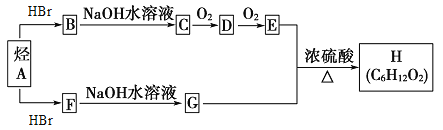
已知:
①R-CH2X![]() R-CH2OH(X代表卤素原子)。
R-CH2OH(X代表卤素原子)。
②在一定条件下,有机物有下列转化关系:
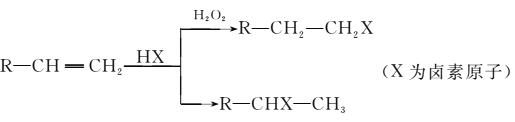
③烃A和等物质的量HBr在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
(1)D的结构简式为_____________。
(2)烃A→B的化学反应方程式为:_____________。
(3)F→G的反应类型:_______________。
(4)E+G→H的化学反应方程式:________________。
(5)H有多种同分异构体,其中能与NaHCO3溶液反应产生气体,且其烃基上的一氯代物有两种的是(用结构简式表示):____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅及其化合物有着优异的性能和广泛的应用。工业上利用铅浮渣(主要成分是PbO、Pb,还含有少量的Ag、CaO)制备硫酸铅。制备流程图如下
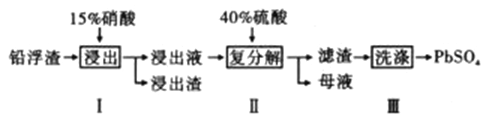
已知:Ksp(PbSO4)=1.6×10-8 Ksp(CaSO4)=4.9×10-5
(1)步骤I有NO产生浸出液中含量最多的金属阳离子为Pb2+,写出Pb参加反应的化学方程式___________________________,为防止Ag被溶解进入溶液,步骤I操作时应注意_______________________。
(2)粗PbSO4产品含有的杂质是____________;要得到纯净的PbSO4,需要用试剂进行多次洗涤,再用蒸馏水洗涤。最好选用的试剂是_________________。
A.稀硫酸 B.稀盐酸 C.硝酸铅溶液 D.酒精
(3)母液可循环利用的物质是HNO3,若母液中残留的SO42-过多,循环利用时可能出现的问题是______________________________。
(4)若将步骤Ⅱ中的Pb2+完全沉淀,则溶液中的c(SO42-)至少为___________mol/L。
(5)(CH3COO)2Pb是皮毛行业可溶于水的染色助剂,可用PbSO4与CH3 COONH4反应制备,写出该反应的离子方程式_______________________。
(6)铅蓄电池是电压稳定、使用方便的二次电池。PbSO4在其中扮演了重要角色,写出铅蓄电池充电时阳极的电极反应_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)为白色晶体,是强氧化剂,常用作火箭发射的推进剂。已知:①NH4ClO4在400℃时开始分解,产物为N2、Cl2、O2、H2O;②Mg3N2易水解。请用下图所示装置设计实验证明分解产物中含有Cl2、H2O以及装置A中生成了Mg3N2(装置不重复使用)。
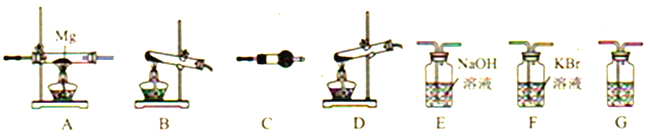
(1)写出高氯酸铵分解的化学方程式__________。
(2)高氯酸铵分解选择的装置是__________(填字母)。
(3)按气流从左到右,装置的连接顺序是:分解装置→_____→_____→_____→_____→_____。______________
(4)C中所放的试剂是__________,G的作用是__________ 。
(5)能证明有Cl2产生的现象是__________。
(6)要证明装置A中生成了Mg3N2需要进行的实验操作以及对应的实验现象是__________。
(7)某实验宣存放的高氯酸铵样品中含有少量杂质,已知可用蒸馏法测定NH4ClO4的含量,其测定流程如下(杂质不参加反应),则样品中NH4ClO4的含量(w)为__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com