
| A. | 负极反应式为:Li-e-=Li+ | |
| B. | 正极反应式为:FeS2+4e-=Fe+2S2- | |
| C. | 电池放电时K+向正极移动 | |
| D. | 可用KCl、LiCl的水溶液做电解质溶液 |
分析 A、负极锂发生氧化反应;
B、正极是FeS2发生还原反应,生成单质铁和-2价的硫离子;
C、原电池中阳离子向正极移动;
D、金属锂可以和水之间发生反应.
解答 解:A、负极锂发生氧化反应,电极反应式为:Li-e-=Li+,故A正确;
B、正极是FeS2发生还原反应,生成单质铁和-2价的硫离子,所以电极反应式为:正极反应式为:FeS2+4e-=Fe+2S2-,故B正确;
C、原电池中阳离子向正极移动,所以钾离子向正极移动,故C正确;
D、金属锂可以和水之间发生反应,所以该电池不能用某物质的水溶液作为电解质溶液,故D错误.
故选D.
点评 本题考查了氧化还原反应、原电池原理,侧重于基础知识的考查,注意根据氧化还原反应中元素化合价的变化分析,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A | B | C |
| D |
| A. | 原子半径由大到小的顺序为E>B>D>C>A | |
| B. | 元素D可形成多种酸,它们的酸根均能促进水的电离 | |
| C. | EB2中存在离子键与非极性共价键 | |
| D. | C位于周期表中第二周期第ⅦA族,其最高正价为+7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子的半径:Z>R>W>Y | |
| B. | Y、Z、W 三种元素组成的化合物的水溶液可能显碱性 | |
| C. | Z 与 Y、Z 与 W 形成的化合物的化学键完全相同 | |
| D. | WY2、Y3 等可作为新的自来水消毒剂替代 W2,主要原因是 WY2、Y3 的氧化性比 W2 更强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若图中反应均为氧化还原反应,当W为金属单质时,则Z可能是FeCl3 | |
| B. | 若图中反应均为氧化还原反应,当W为非金属单质时,则Z可能是CO2 | |
| C. | 若图中反应均为非氧化还原反应,当W为一元强酸时,则X可能是NH3 | |
| D. | 若图中反应均为非氧化还原反应,当W为一元强碱时,则X可能是NaAlO2 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省徐州市高二上第一次月考化学试卷(解析版) 题型:填空题
(1)已知下列两个热化学方程式:
C3H8(g)+5O2(g) 3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1
H2O(l) H2O(g) ΔH=+44.0 kJ·mol-1
则0.5 mol丙烷燃烧生成CO2和气态水时释放的热量为 。
(2)已知:TiO2(s)+2Cl2(g) TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g) 2CO(g) ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如右图所示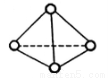 ),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN
),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________kJ能量。
(4)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:
2H2+O2 2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将___________能转化为__________能。其电极反应式分别为:负极_________________,正极____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NOx、SO2、CO等大气污染气体的处理具有重要意义.有学者想以如图所示装置用原电池原理将SO2转化为重要的化工原料.下列说法不正确的是( )
随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NOx、SO2、CO等大气污染气体的处理具有重要意义.有学者想以如图所示装置用原电池原理将SO2转化为重要的化工原料.下列说法不正确的是( )| A. | 溶液中H+的移动方向由A极到B极 | |
| B. | 电池总反应方程式为:2SO2+O2+2H2O=2H2SO4 | |
| C. | 正极电极反应式为:SO2+2H2O-2e-=SO42-+4H+ | |
| D. | 当有0.25mol SO2被吸收时,通过H+交换膜的H+的物质的量为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
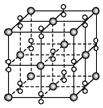
| A. | 该晶体为分子晶体 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 每个晶胞含有4个Ba2+和4个O2- | |
| D. | 与每个Ba2+距离相等且最近的Ba2+共有12个 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省徐州市高二上第一次月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.0.1 mol Cl2全部溶于水后转移电子的数目为0.1NA
B.标准状况下,0.56 L丙烷中含有共价键的数目为0.2NA
C.常温常压下,14 g C2H4、C3H6的混合气体中含有碳原子的数目为NA
D.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com