

 N2
N2  NO;则A为 NH3,根据变化书写化学方程式,以此书写电子式和结构式;
NO;则A为 NH3,根据变化书写化学方程式,以此书写电子式和结构式; Al(OH)3
Al(OH)3  AlO2-,则反应(Ⅲ)的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓;
AlO2-,则反应(Ⅲ)的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓; Na2CO3
Na2CO3 NaHCO3;②将等物质的量的Na2CO3,NaHCO3溶于水形成混合溶液,由于CO32-离子水解生成HCO3-离子,故c(HCO3-)>c(CO32-),Na2CO3,NaHCO3水解呈碱性,故c(OH-)>c(H+),水解的程度只是少部分,故c(CO32-)>c(OH-),以此判断离子浓度大小.
NaHCO3;②将等物质的量的Na2CO3,NaHCO3溶于水形成混合溶液,由于CO32-离子水解生成HCO3-离子,故c(HCO3-)>c(CO32-),Na2CO3,NaHCO3水解呈碱性,故c(OH-)>c(H+),水解的程度只是少部分,故c(CO32-)>c(OH-),以此判断离子浓度大小. N2
N2  NO;则A为 NH3,发生反应的化学方程式为4NH3+3O2=2N2+6H2O; B为氮气结构式为N≡N,
NO;则A为 NH3,发生反应的化学方程式为4NH3+3O2=2N2+6H2O; B为氮气结构式为N≡N, FeCl3
FeCl3 FeCl2;HNO3
FeCl2;HNO3 Fe(NO3)3
Fe(NO3)3 Fe(NO3)2;FeCl3 或Fe(NO3)3加热蒸干溶液得到Fe(OH)3;继续灼烧后得到的固体物质为Fe2O3,
Fe(NO3)2;FeCl3 或Fe(NO3)3加热蒸干溶液得到Fe(OH)3;继续灼烧后得到的固体物质为Fe2O3, Al(OH)3
Al(OH)3  AlO2-,则反应(Ⅲ)的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
AlO2-,则反应(Ⅲ)的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓; Na2CO3
Na2CO3 NaHCO3;
NaHCO3;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
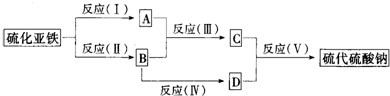
 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图所示(部分反应中的水已略去).
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图所示(部分反应中的水已略去). Fe(OH)3+3H+
Fe(OH)3+3H+ Fe(OH)3+3H+
Fe(OH)3+3H+查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com