
����Ŀ�������й�֪ʶ�ش��������⡣
�����о�CO2�����þ�����ʵ���壬���罫CO2�뽹̿��������CO��CO���������������ȼ�ϵ�صȡ�
��1����֪��Fe2O3(s)+3C��ʯī��=2Fe(s)+3CO(g) ��H 1 =+489 kJ/mol
C��ʯī��+CO2(g)=2CO(g) ��H 2 = +172 kJ/mol
д��Fe2O3��COΪԭ��ұ�������Ȼ�ѧ����ʽ___________________________��
��2������COȼ�շ�Ӧ����Ƴ�CO/O2ȼ�ϵ��(��H2SO4��ҺΪ�������Һ),д���õ�ص�������Ӧʽ_____________________________________��
������������ѧ��ͭ������ϡ���ᷴӦ��ijѧ����������CO/O2ȼ�ϵ���������ͼ��ʾװ�ã����ڲ���δ������,ʵ����ͭ��ϡ����ķ�Ӧ��Cu+H2SO4=H2��+CuSO4(δע����Ӧ����)���ش��������⡣
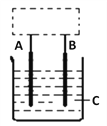
��3��A��ʯī����B��һ�ֽ������ý�����________(������)��
��4��BӦ�ӵ�Դ��________��������ͨ��CO������ͨ��O2������
��5��д����װ���з�����ԭ��Ӧ�ĵ缫��Ӧʽ___________________________________��
��6����C��ҺΪ100mL����ʳ��ˮ,A��B�缫��Ϊʯī������ѧ����ͨ��·��д���ձ��з�Ӧ�����ӷ���ʽ_________________�����ų������112mL����ʱ������Һ��pH=_____________�������£���
������������װ�ø������ͼװ��������ģ�����ĵ绯ѧ������

��7����XΪͭ,Ϊ�������ĸ�ʴ������KӦ����______����
��8����XΪп��������K����M��,�õ绯ѧ��������Ϊ________________��
���𰸡� Fe2O3(s)+3CO(g)��2Fe(s)+3CO2(g)��H����27kJ/mol O2+ 4H++ 4e���� 2H2O ͭ ͨ��O2 2H++2e����H2�� 2Cl-+2H2O![]() 2OH-+H2��+Cl2�� 13 N �� ��������������������
2OH-+H2��+Cl2�� 13 N �� ��������������������
��������(1)��֪��a��Fe2O3(s)+3C(ʯī)=2Fe(s)+3CO(g)��H1=+489.0kJmol-1��b��C(ʯī)+CO2(g)=2CO(g)��H2=+172kJmol-1�����ݸ�˹����a-b��3�õ���Fe2O3(s)+3CO(g)�T2Fe (s)+3CO2(g)��H=489-172��3=-27kJ/mol���ʴ�Ϊ��Fe2O3(s)+3CO(g)��2Fe(s)+3CO2(g) ��H��-27kJ/mol��
(2)CO-O2ȼ�ϵ��(��H2SO4��ҺΪ���Һ)��һ����̼�ڸ���ʧ���ӷ���������Ӧ���ɶ�����̼��ԭ��ظ����缫��ӦΪ��CO+H2O-2e-=CO2+2H+�������缫��ӦΪ�����õ����ӷ�����ԭ��Ӧ����������Һ�еĵ缫��ӦΪ��O2+4H++4e-=2H2O���ʴ�Ϊ��O2+4H++4e-=2H2O��
(3)Ҫʵ��ͭ��ϡ����ķ�Ӧ��Cu+H2SO4=H2��+CuSO4��ֻ�����õ��ԭ����A��ʯī����B��һ�ֽ�����ֻ����ͭ���ʴ�Ϊ��ͭ��
(4)���ݷ�Ӧ����ʽ��ͭ�����������BӦ�ӵ�Դ����������ͨ��O2��һ�����ʴ�Ϊ��ͨ��O2��
(5)��װ�ã���Һ�е�������������������ԭ��Ӧ�����������缫��ӦʽΪ2H++2e����H2�����ʴ�Ϊ��2H++2e����H2����
(6)��ʯī���缫��ⱥ���Ȼ�����Һʱ�������������ӷŵ����������������������ӷŵ�����������ͬʱ�����������������������ɣ���ط�ӦʽΪ2Cl-+2H2O![]() H2��+Cl2��+2OH-�����������������ӵ����ʵ���Ϊx��
H2��+Cl2��+2OH-�����������������ӵ����ʵ���Ϊx��
2Cl-+2H2O![]() H2��+Cl2��+2OH-��
H2��+Cl2��+2OH-��
22.4L 2mol
0.112L x
22.4L��2mol=0.112L��x����ã�x=![]() =0.01mol��c(OH-)=
=0.01mol��c(OH-)=![]() =0.1mol/L������Һ��pH=13���ʴ�Ϊ��2Cl-+2H2O
=0.1mol/L������Һ��pH=13���ʴ�Ϊ��2Cl-+2H2O![]() 2OH-+H2��+Cl2����13��
2OH-+H2��+Cl2����13��
(7)��XΪͭ��Ϊ�������ĸ�ʴ������ͭ���ã�����Ҫ������ӵ���������������������Ϊ�ӻ�����ʴ��KӦ����N�����ʴ�Ϊ��N����
(8)��XΪп������K����M�����÷���Ϊ�����������������������ʴ�Ϊ������������������������


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪100��ʱ��ˮ�����ӻ�����Kw=1��10-12,���ڸ��¶���pH=l1�İ�ˮ������������ȷ����
A. �����Һ�м���ͬ��ͬ���pH=1�����ᣬ��Ӧ����Һ������
B. �¶Ƚ�����25��,�ð�ˮ��Һ��H2O�������H+Ũ��С��10-11mol/L
C. �ð�ˮ��Һ�м���NH4Cl��Һ��NH3��H2O�ĵ���������ǿ
D. �μӵ�Ũ�ȵ���������ᣬ�õ�����Һ�д��ڵ���ƽ��:NH4HSO4(aq)![]() NH4+(aq)+H+(aq)+SO42-(aq)
NH4+(aq)+H+(aq)+SO42-(aq)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���ܱ��������м���һ�����ɻ����ĸ���(��Ȳ���)�������ֳ������֣�����߳���1molN2���ұ߳���һ������COʱ�����崦����ͼλ��(�����¶Ȳ���)������˵����ȷ����( )
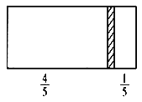
A���ұ�����߷�����֮��Ϊ4:1
B���Ҳ�CO������Ϊ5.6 g
C���Ҳ������ܶ�����ͬ�����������ܶȵ�14��
D�����ı��ұ�CO�ij�������ʹ���崦���������м䣬�����¶Ȳ��䣬��Ӧ����22.4 L��CO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. 1mol/L��Na2CO3��Һ�к���������ԼΪ2��6.02��1023
B. ����ԭ������ΪNA��O2��O3�����ʵ���֮��Ϊ3��2
C. ÿ1mol�κ����ʾ�����ԼΪ6.02��1023��ԭ��
D. ����ԭ����Ŀ��ͬ��NH3��CH4��ͬ��ͬѹ�µ����֮��Ϊ3��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���������ʣ����������ڳ���ʯ��ˮ����ˮ������ϡ���ᣬ���Ȼ�ͭ���壬�������������ƣ������ǣ����ƾ�����������̼�������ᱵ���������ڵ���ʵ���______������ţ�������ͬ�������ڷǵ���ʵ���_________���ܵ������_________��
��2��д������������ȷֽ��������Ļ�ѧ��Ӧ����ʽ____________________����Ӧ�е���������________����ԭ������____________������2mol����ת��ʱ�����ɵ������ڱ�״���µ������________L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N��P��As��Ԫ�صĻ��������������о�����������Ҫ��;����ش�����������
��1�������������ѧ��[FuNvio Cacace���˻���˼��������о������N4���ӣ��÷��ӵĿռ乹����P4���������е�ԭ�ӵĹ���ӻ���ʽΪ__________��N-N���ļ���Ϊ__________��
��2����̬��ԭ�ӵļ۵����Ų�ͼΪ__________������ͬ��������Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ__________��
��3����λԭ���Թ¶Ե�����������Խ��������Խ��������ɽ����γ�����PH3��NH3�Ľṹ�����������������������γ���������__________(��"PH3������NH3��)��
��4��SCl3+��PCl3�ǵȵ����壬SCl3+�Ŀռ乹����__________��S-Cl������__________P-Cl������__________(������������=����������)��ԭ����__________��
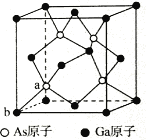
��5���黯��Ϊ������������������Ϊ��������ĵ����������������١���֪�����黯�������Ľṹ��ͼ��ʾ���黯���Ļ�ѧʽΪ__________�������������ܶ�Ϊ��gcm-3����NAΪ�����ӵ�������ֵ����a��b�ľ���Ϊ__________pm(�ú�����NA�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֬�����̶Ⱦ�������֬�ij�Ĥ�ԡ�������һ�ֳ�Ĥ�����õĴ�������֬�ĺϳ�·�ߣ�����ͼ��ʾ��
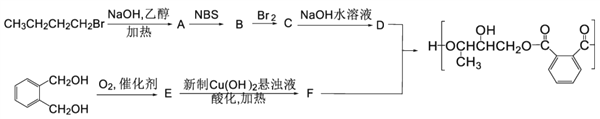
(1)B�ķ���ʽΪC4H7Br����B������˳���칹��B�Ľṹ��ʽΪ________��A��B����ķ�Ӧ������_________��
(2)E�к��������ŵ�������_________��D��ϵͳ����Ϊ_________��
(3)����˵����ȷ����_________��
A.1 mol������C�������3 mol NaOH
B��1 mol������E������������Һ��Ӧ����2 mol Ag
C��F������Cu(OH)2����Һ��Ӧ
D�����顢1-������������D�зе���ߵ��Ƕ���
(4)д��D��F��һ�����������ɴ�������֬�Ļ�ѧ����ʽ_________��
(5) 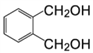 �ķ�������������ͬ���칹����_______�֡�
�ķ�������������ͬ���칹����_______�֡�
�ٱ��Ķ�ȡ�����������FeCl3��Һ����ɫ���ۿɷ�����ȥ��Ӧ
(6)�ټ�֪������������ܷ������·�Ӧ��

��C2H5OH+HBr��C2H5Br+H2O
����������Ӧԭ�����Ա������������1,3-���������Ҵ���Ϊԭ�Ϻϳ�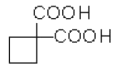 ��������Ƴ������ķ�Ӧ����ͼ__________________��
��������Ƴ������ķ�Ӧ����ͼ__________________��
��ʾ���ٺϳɹ��������Լ���ѡ���ںϳɷ�Ӧ����ͼ��ʾ����ʾ�����£�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�������ͼʵ��װ��̽����������ʣ�����ͼʾ�ж����н��۲���ȷ����
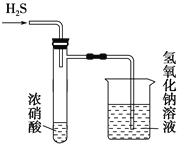
A. �Թ��ڱ��ϵġ���˪���ijɷ�����
B. ��ʵ���˵����Ũ������������ԣ���˵����Ũ������лӷ���
C. �ձ�������������Һ�������dz�ȥβ������ֹβ����Ⱦ����
D. �Թ���Ũ���������Ũ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������H2RO4=H++HRO4-��HRO4-![]() H++RO42-,�������ʵ���Ũ�ȶ�Ϊ0.1mol/L��������Һ:��NaHRO4��Һ; ��H2RO4��Һ; ��Na2RO4��Һ������˵����ȷ����
H++RO42-,�������ʵ���Ũ�ȶ�Ϊ0.1mol/L��������Һ:��NaHRO4��Һ; ��H2RO4��Һ; ��Na2RO4��Һ������˵����ȷ����
A. �ں͢۵������Ϻ����Һ��: c( Na+)= c( HRO4-)+c(H2RO4) +c(RO42-)
B. 100mL����Һ��: n(HRO4-)+n(RO42-)+n(OH-)-n(H+)= 0.01
C. �ٺ͢ڵ������Ϻ����Һ�п��ܵ�����Ũ��Ϊc( HRO4-)>c(H+)>c(Na+)
D. ���ٺ͢۵������Ϻ�����ˮ�ĵ��룬��HRO4-�ĵ���̶ȿ϶�����RO42-��ˮ��̶�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com