


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、11.2L NO和11.2L O2混合后的分子总数为NA |
| B、1mol苯乙烯中含有的碳碳双键数为4NA |
| C、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| D、1mol Fe与足量的稀HNO3反应并放出NO和N2O,转移3NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2013年我国煤炭产量35.2亿吨,约占一次能源生产总量78.6%;煤炭消费总量35.7亿吨,约占一次能源消费总量72.8%.中国富煤缺油少气的能源资源状况决定了在今后较长时期内,煤炭仍将是中国的主要能源.
2013年我国煤炭产量35.2亿吨,约占一次能源生产总量78.6%;煤炭消费总量35.7亿吨,约占一次能源消费总量72.8%.中国富煤缺油少气的能源资源状况决定了在今后较长时期内,煤炭仍将是中国的主要能源.| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选用试剂 | 实验现象 | |
| 第一种方法 | ||
| 第二种方法 |
| 实验步骤 | 实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
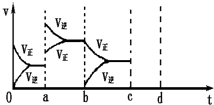 (1)如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是
(1)如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、实验室用氯化铁溶液制取氢氧化铁胶体:Fe3++3H2O
| ||||
| B、碳酸钙溶于醋酸:CaCO3+2H+═Ca2++H2O+CO2↑ | ||||
| C、铝和烧碱溶液:2Al+2OH-+2H2O═2Al3++3H2↑ | ||||
| D、AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com