
【题目】回答下列问题:
(1)写出泡沫灭火器的灭火原理的离子方程式
(2)已知25℃,101 kPa时:
S(s)+O2(g)==SO2(g) H=-296.8 kJ/mol
2Cu(s)+O2(g)==2CuO(s) H=-314.6 kJ/mol
Cu(s)+S(s)==CuS(s) H=-53.1 kJ/mol
写出CuS(s)与O2(g)反应生成CuO(s)和SO2(g)的热化学方程式 。
(3)已知常温下AI(OH)3的Ksp=l.0×10-33,若溶液中c(Al3+)为1.0 mol/L,请计算Al3+开始沉淀的pH= 。常温下,浓度均为0.01mol/L的CH3COOH和CH3COONa的混合液中,PH = a,则醋酸的电离常数约为Ka = 。
(4)在常温下,向V L pH=12的Ba(OH)2溶液中逐滴加入一定浓度的NaHSO4稀溶液,当溶液中的Ba2+ 恰好沉淀完全时,溶液pH=11。则Ba(OH)2溶液与NaHSO4溶液的体积比为 ,NaHSO4溶液的物质的量浓度为 mol/L。
【答案】(1)Al3++3HCO3—=Al(OH)3↓+3CO2↑
(2)2CuS(s)+3O2(g)==2CuO(s)+2SO2(g)ΔH=-802.0kJ/mol
或CuS(s)+![]() O2(g)==CuO(s)+SO2(g)ΔH=-401.0kJ/mol
O2(g)==CuO(s)+SO2(g)ΔH=-401.0kJ/mol
(3) 3 10—a (4)1:4,1.25×10﹣3molL﹣1
【解析】
试题分析:(1)泡沫灭火器是利用Al3+ 和HCO3—发生 双水解反应,发生反应的离子方程式为Al3+ +3HCO3— = Al(OH)3↓+ 3CO2↑;
(2)已知①S(s)+O2(g)==SO2(g) H=-296.8kJ/mol
②2Cu(s)+O2(g)==2CuO(s) H=-314.6kJ/mol
③Cu(s)+S(s)==CuS(s) H=-53.1kJ/mol
根据盖斯定律可知由①×2+②-③×2得2CuS(s)+3O2(g) ==2CuO(s)+2SO2(g),
则ΔH =(-296.8kJ/mol×2)+(-314.6kJ/mol)-(-53.1kJ/mol×2)=-802.0kJ/mol,此反应的热化学方程式为2CuS(s)+3O2(g) ==2CuO(s)+2SO2(g) ΔH =-802.0kJ/mol;
(4)VL pH=12的Ba(OH)2溶液中c(OH-)=10-2mol/L,含有的氢氧根离子物质的量为V×10-2mol=0.01Vmol,溶液中的Ba2+恰好完全沉淀时反应的硫酸氢钠物质的量为0.5V×10-2mol=0.005Vmol,设硫酸氢钠溶液体积为x,依据反应Ba(OH)2+NaHSO4=BaSO4↓+H2O+NaOH,混合后溶液pH=11,反应后的溶液中氢氧根离子浓度为:c(OH-)=10-3mol/L,则:![]() =10-3,解得:x=4VL,
=10-3,解得:x=4VL,
则Ba(OH)2溶液与NaHSO4溶液的体积比为VL:4VL=1:4;
该硫酸氢钠溶液的浓度为:![]() =1.25×10-3 molL-1。
=1.25×10-3 molL-1。


科目:高中化学 来源: 题型:
【题目】关于物质的类别,下列说法正确的是
A.食盐水、糖水和冰水都是饮料,属于混合物
B.O2不能导电,故O2是非电解质
C.烧碱属于碱,纯碱属于盐
D.NaHSO4能电离出氢离子,故NaHSO4属于酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。
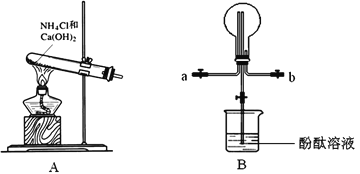
请回答:
(1)实验室制备氨气的化学方程式为 ;干燥氨气常用的干燥剂是 。
(2)收集氨气时,请你选择氨气的进气口 (填“a”或“b”),理由是 。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是 。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是 ( 填序号)。
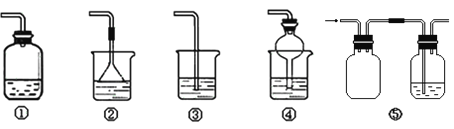
(5)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年11月5 日,长征三号乙运载火箭将两颗北斗三号全球导航卫星送入太空轨道。下列有关说法正确的是
A. 火箭燃料中的四氧化二氮属于化石燃料 B. 火箭燃料燃烧时将化学能转化为热能
C. 火箭箭体采用铝合金是为了美观耐用 D. 卫星计算机芯片使用高纯度的二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 25℃时 Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度
B. 常温下,NaClO溶液显碱性的原因:ClO—+ H2O =" HClO" + OH—
C. 2NO(g) + 2CO(g) = N2(g) + 2CO2(g),在常温下能自发进行,则该反应的△H >0
D. 25℃时向水中加入少量NaOH后,由水电离出的c(H+)c(OH—)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】U、V、W、X、Y、Z是原子序数依次增大的短周期元素。已知:
①WU4++XU-==WU3+U2X,各种反应物和生成物的电子总数都与Y+相等;
②Z的单质在X2中燃烧的产物可使品红溶液褪色;
③V的单质在X2中燃烧可生成VX和VX2两种气体;
④Y的单质是一种金属,该金属与X2反应可生成Y2X和Y2X2两种固体。
请回答下列问题:
(1)写出Y2X2与水反应的化学方程式:________________。
(2)V、W、X形成的10电子氢化物中,沸点最高的是__________(写化学式)。
(3)U2X2与FeSO4按物质的量之比1:2溶于稀硫酸中,反应的离子方程式为__________。
(4)常温下,向pH=11的Y2VX3溶液中加入过量石灰乳,过滤后所得溶液pH=13,则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是_________。
(5)已知由U、W两种元素组成的共价化合物联氨的球棍模型如图所示,则联氨分子的电子式为____________。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为_______(已知:N2H4+H+==N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与过量硫酸形成的酸式盐的化学式为______________。
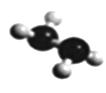
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,组成一种原电池。试回答下列问题(灯泡功率合适):
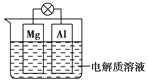
(1)电解质溶液为稀硫酸时,灯泡________ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Mg电极上发生的反应为______________;Al电极上发生的反应为________________________________________________________________________。
(2)电解质溶液为NaOH溶液时,灯泡________ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,Al电极上发生的反应为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中加入足量Na2O2后仍能大量共存的离子组是( )
A.NH4+、Ba2+、Cl﹣、NO3﹣
B.K+、AlO2﹣、Cl﹣、SO42﹣
C.Ca2+、Mg2+、NO3﹣、HCO3﹣
D.Na+、Cl﹣、CO32﹣、SO32﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com