
下列表示对应化学反应的离子方程式正确的是()
A. 漂白粉露置在空气中失效:ClO﹣+CO2+H2O=HClO+HCO3﹣
B. 向NaAlO2溶液中通入过量CO2:AlO2﹣+CO2+2H2O=Al(OH)3↓+HCO3﹣
C. 用过氧化氢从酸化的海带灰浸出液中提取碘:2I﹣+H2O2+2H+═I2+2H2O
D. 过氧化钙固体与水反应:2O22﹣+2H2O=4OH﹣+O2↑
考点: 离子方程式的书写.
专题: 离子反应专题.
分析: A.漂白粉的有效成分为次氯酸钙,次氯酸钙与二氧化碳反应生成碳酸钙沉淀和次氯酸;
B.二氧化碳过量,反应生成碳酸氢根离子;
C.过氧化氢能够将碘离子氧化成碘单质,根据电子守恒和质量守恒定律判断;
D.过氧化钙不能拆开,需要保留化学式.
解答: 解:A.Ca(ClO)2是漂白粉中有效成分,漂白粉置于空气中易失效的原因是发生Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO,2HClO 2HCl+O2↑反应,离子方程式为:Ca2++2ClO﹣+H2O+CO2=CaCO3↓+2HClO,故A错误;
2HCl+O2↑反应,离子方程式为:Ca2++2ClO﹣+H2O+CO2=CaCO3↓+2HClO,故A错误;
B.向NaAlO2溶液中通入过量CO2,反应生成的是碳酸氢根离子,离子方程式为:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣,故B正确;
C.用过氧化氢从酸化的海带灰浸出液中提取碘,反应的离子反应为:2I﹣+H2O2+2H+═I2+2H2O,故C正确;
D.过氧化钙与水反应的化学方程式为:2CaO2+2H2O=2Ca(OH)2+O2↑,过氧化钙不能拆开,正确的离子方程式为:2CaO2+2H2O=2Ca2++4OH﹣+O2↑,故D错误;
故选BC.
点评: 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒、电子守恒和电荷守恒等).


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源: 题型:
某待测溶液(阳离子为Na+)中可能含有SO42﹣、SO32﹣、NO3﹣、C1﹣、Br﹣、S2﹣、CO32﹣、HCO3﹣中的一种或多种,进行如图所示的实验,每次实验所加试剂均过量,回答以下问题: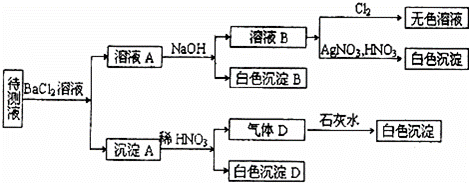
(1)待测液中是否含有SO42﹣、SO32﹣: .
(2)沉淀B的化学式为 ;生成沉淀B的离子方程式为 .
(3)根据以上实验,待测液中肯定没有的离子是 ;肯定存在的离子还有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应①KHCO3溶液与石灰水反应;②Na2CO3 溶液与稀盐酸反应;③Na与烧碱溶液反应;④Fe与稀硝酸反应;改变反应物用量或浓度,不能用同一个离子方程式表示的是()
A. ①②③ B. ①②④ C. ①③④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
铁单质及其化合物在生活、生产中应用广泛.请回答下列问题:
(1)由于氧化性Fe3+>Cu2+,氯化铁溶液常用做印刷电路铜板腐蚀剂,反应的离子方程式是 .
(2)硫酸铁可做絮凝剂,常用于净水,其原理是
(用离子方程式表示).在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是 .
(3)磁铁矿冶炼铁的原理是Fe3O4+4CO=3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移的电子的物质的量是 .
(4)表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是B(填字母).
选项 陈述Ⅰ 陈述Ⅱ 判断
A 铁是地壳中含量最高的金属元素 铁是人类最早使用的金属材料 Ⅰ对;Ⅱ对;有
B 常温下铁与稀硫酸反应生成氢气 高温下氢气能还原氧化铁得到铁 Ⅰ对;Ⅱ对;无
C 铁属于过渡元素 铁和铁的某些化合物可用做催化剂 Ⅰ错;Ⅱ对;无
D 在空气中铁的表面能形成致密的氧化膜 铁不能与氧气反应 Ⅰ对;Ⅱ对;有
查看答案和解析>>
科目:高中化学 来源: 题型:
元素A和B的原子序数都小于18.已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M电子层数为(a﹣b),L层电子数为(a+b),则A、B两元素所形成的化合物的性质可能有()
A. 能与水反应 B. 能与氢氧化钠反应
C. 能与硫酸反应 D. 不能与碳酸钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某碱性溶液中只含有Na+、CH3COO﹣、H+、OH﹣四种离子.下列描述正确的是()
A. 该溶液可能由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
B. 该溶液一定由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合而成
C. 该溶液中离子浓度一定为c(Na+)>c(CH3COO﹣)>c(OH﹣)>c(H+)
D. 加入一定量冰醋酸,c(CH3COO﹣)可能大于、等于或小于c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应A(g)+3B(g)⇌2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是()
A. v(A)=0.01 mol/(L•s) B. v(B)=0.04 mol/(L•s)
C. v(B)=0.60mol/(L•min) D. v(C)=1.0mol/(L•min)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于化合反应,又属于氧化还原反应的是( )
|
| A. | Fe+2HCl=FeCl2+H2↑ | B. | 2FeCl2+Cl2=2FeCl3 |
|
| C. | CaO+H2O=Ca(OH)2 | D. | 2Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法正确的是()
A. 除去乙烷中少量的乙烯:光照条件下通入Cl2,使乙烯转化成液态二氯乙烷而与乙烷分离
B. 除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤,分液、干燥、蒸馏
C. 除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶
D. 除去乙醇中少量的乙酸:加足量生石灰,蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com