
| A. | 增加6.5g | B. | 减少6.5g | C. | 减少5.6g | D. | 增加6.4g |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 加热氧化银 | B. | 煅烧碳酸钙 | ||
| C. | 电解氯化钠溶液 | D. | 氯化镁与铝粉高温共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
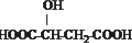
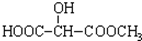 B.
B. C.H3COOC-COOCH3
C.H3COOC-COOCH3 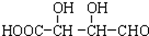 E.
E.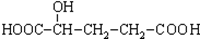
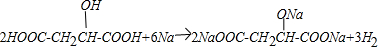 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
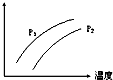 如图表示温度、压强对达平衡的可逆反应:2L(g)?2M(g)+N(g)△H>0的影响(P1<P2)图中y轴表示的意义是( )
如图表示温度、压强对达平衡的可逆反应:2L(g)?2M(g)+N(g)△H>0的影响(P1<P2)图中y轴表示的意义是( )| A. | 混合物中L的百分含量 | B. | 混合气体的密度 | ||
| C. | L的转化率 | D. | 混合气体的平均分子量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用瓷坩埚高温熔融NaOH | |
| B. | 用氨气做喷泉实验主要是利用氨气的水溶液呈碱性这一性质 | |
| C. | 碳酸钠的溶解性比碳酸氢钠大 | |
| D. | 检验Fe2+用KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应及离子方程式 | 评价 |
| A | NaClO溶液中通往少量的SO2: ClO-+H2O+SO2=Cl-+SO42-+2H+ | 错误,碱性介质中不可能生成H+ |
| B | 用酸性高锰酸钾溶液滴定草酸: 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O | 正确 |
| C | NH4Al(SO4)2溶液中滴入少量NaOH溶液 NH4++OH-=NH3•H2O | 错误,OH-首先和Al3+反应生成Al(OH)3沉淀 |
| D | 用惰性电极电解CuCl2溶液 2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | 正确 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com