
| A. | 混合气体的压强 | |
| B. | 混合气体的密度 | |
| C. | 气体的总物质的量 | |
| D. | 单位时间内生成nmolC的同时消耗2nmolB |
分析 反应到达平衡状态时,正逆反应速率相等,平衡时各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,由此进行判断.
解答 解:A.该反应是一个反应前后气体体积不变的化学反应,无论反应是否达到平衡状态,容器中气体的压强始终不变,所以不能证明达到了平衡状态,故A错误;
B. 由于A是固体,反应两边气体的质量不相等,容器的体积不变,混合气体密度不变,说明各组分的浓度不变,达到了平衡状态,故B正确;
C.由于反应两边气体的化学计量数相等,物质的量始终不变,所以物质的量不变不能判断是否达到了平衡状态,故C错误;
D.单位时间内生成n mol C的同时消耗2n molB,表示的都是正逆反应速率,不能判断正逆反应速率是否相等,故D错误;
故选B.
点评 本题考查化学平衡状态判断,为高频考点,注意:只有反应前后改变的物理量才能作为判断化学平衡的依据,反应前后不改变的物理量不能作为化学平衡的判断依据,本题难度不大.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:选择题
| A. | m=-26.5 2c=a-b | B. | m=-53 c2=$\frac{a}{b}$ | C. | m=-26.5 c2=$\frac{a}{b}$ | D. | m=-53 2c=a-b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向2.0mL浓度均为0.lmol•L-l的KC1、KI混合溶液中滴加1~2滴0.0lmol/LAgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比Agl的Ksp大 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入适量的H2O2,铜粉仍不溶解 | |
| C. | 向AIC13溶液中滴加氨水,产生白色沉淀;再加入NaHSO4溶液,沉淀不消失 | |
| D. | 将CO2通入Ba(NO3)2溶液中至饱和,无沉淀产生;再通入SO2,也无沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
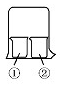 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( ) | ①中的物质 | ②中的物质 | 预测①的现象 | |
| A | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
| B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
| C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
| D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
| A. | 淀粉KI溶液浓硝酸无明显变化 | B. | 酚酞溶液浓盐酸无明显变化 | ||
| C. | AlCl3溶液浓氨水有白色沉淀 | D. | 湿润红纸条饱和氯水红纸条褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
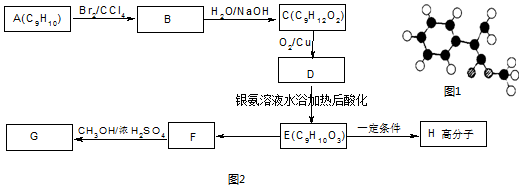
 ,G的一种同分异构体的结构简式为
,G的一种同分异构体的结构简式为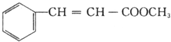 .
.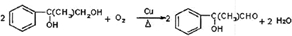
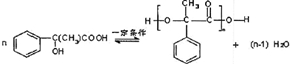 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
| 质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
| 沸点/℃ | 57.6 | 31.8 | 8.2 | -85 | 12.5 | 75.5 |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com