
 用化学用语回答下面的问题
用化学用语回答下面的问题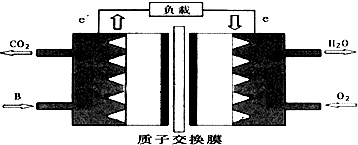
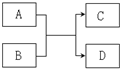
分析 (1)通常若A为黄绿色单质,应为Cl2,B为无色液态化合物,应为H2O,二者反应生成HCl和HClO;
(2)若B为化合物,且A、C两种无色气体相遇变为红棕色,应为NH3和O2的反应;
(3)若A为单质,C、D为常见易燃气体,应为C和H2O的反应,生成H2和CO;
(4)若A为单质,灼烧D产生黄色火焰,说明含有钠元素,B通常是无色液态化合物,如分子含有10个电子,应为H2O,如分子含有18个电子,应为CH3OH.
解答 解:(1)通常若A为黄绿色单质,应为Cl2,B为无色液态化合物,应为H2O,二者反应生成HCl和HClO,B为无色液态化合物,且0.1mol/L的C溶液pH=1,应为HCl,
则D为HClO,D物质的结构式为H-O-Cl,因为ClO-+Cl-+2H+=Cl2↑+H2O,所以ClO-和Cl-在酸性条件下不能大量共存,
故答案为:H-O-Cl;ClO-+Cl-+2H+=Cl2↑+H2O;
(2)若B为化合物,且A、C两种无色气体相遇变为红棕色,应为NH3和O2的反应,则B为NH3,工业上制取B物质的反应为N2+3H2 $?_{高温高压}^{催化剂}$2NH3,氨气溶于水形成氨水,能电离出氢氧根离子,能抑制水的电离,
故答案为:N2+3H2 $?_{高温高压}^{催化剂}$2NH3;氨气溶于水形成氨水,能电离出氢氧根离子,能抑制水的电离;
(3)若A为单质,C、D为常见易燃气体,应为C和H2O的反应,生成H2和CO,反应的化学方程式为C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2,故答案为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
(4)若A为单质,灼烧D产生黄色火焰,说明含有钠元素,
①如B分子含有10个电子,应为H2O,A与B反应为Na和H2O的反应,反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
②如分子含有18个电子,应为CH3OH,A+B→C+D的化学方程式为2Na+2CH3OH=2CH3ONa+H2↑,CH3OH-O2燃料电池中,CH3OH在负极发生氧化反应,电极方程式为2CH3OH+2H2O-12e-=2CO2↑+12H+,
故答案为:2Na+2CH3OH=2CH3ONa+H2↑;2CH3OH+2H2O-12e-=2CO2↑+12H+.
点评 本题考查无机物的推断,题目较为综合,涉及物质的性质、原电池原理以及弱电解质的电离等知识,注意根据物质的性质特点推断物质的种类为解答该题的关键,题目难度中等.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:选择题
| A. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 | |
| B. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 | |
| C. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 | |
| D. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | N | S | O | Si |
| 原子半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
| A. | 0.80×10-10m | B. | 1.20×10-10m | C. | 1.10×10-10m | D. | 0.70×10-10m |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇与浓氢溴酸反应:CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O | |
| B. | 溴乙烷与氢氧化钠溶液共热:CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr | |
| C. | 苯酚钠中通入二氧化碳:2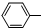 ONa+CO2+H2O→2 ONa+CO2+H2O→2 OH+Na2CO3 OH+Na2CO3 | |
| D. | 淀粉在稀硫酸作用下水解:(C6H10O5)n(淀粉)+nH2O$→_{△}^{稀硫酸}$nC6H12O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{1}^{2}$H和${\;}_{1}^{3}$H | B. | H2O和H2O2 | ||
| C. | CH4和CH3CH3 | D. | 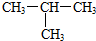 和CH3-CH2-CH2-CH3 和CH3-CH2-CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
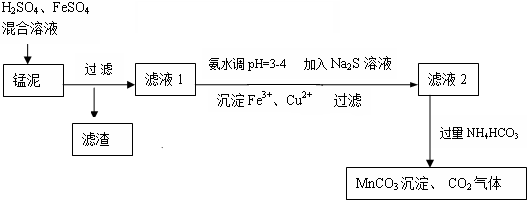
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数是94 | B. | 原子序数是239 | C. | 质量数是94 | D. | 中子数是239 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
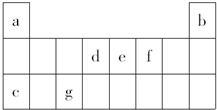 如表是元素周期表中的一部分,表中所列字母分别表示一种元素.(选项中的物质都由下表中的元素组成)由表中信息可推断下列说法正确的是( )
如表是元素周期表中的一部分,表中所列字母分别表示一种元素.(选项中的物质都由下表中的元素组成)由表中信息可推断下列说法正确的是( )| A. | 宇航员在飞船活动舱内会产生d和f组成的气体,吸收这种气体的化合物应该由e和f组成 | |
| B. | 活动舱内还要营造一种适合宇航员生存的人工生态环境,即充入a和f的常见单质 | |
| C. | c和f以原子个数之比为1:1组成的化合物可用作宇航员所需f单质的来源 | |
| D. | 《阿凡达》中潘多拉星球上存在32b,地球上此元素主要以42b形式存在,32b比42b少一个质子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com