
科目:高中化学 来源: 题型:
某气态烃A在标准状况下的密度为1.25 g/L,其产量可以用来衡量一个国家的石油化工发展水平。B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,F有香味。它们之间的转化关系如下图所示:
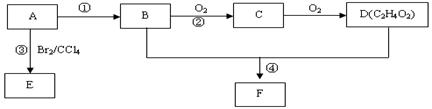
(1)A的结构简式为 ,B中官能团的电子式为 ,
D中官能团的名称为 。
(2)反应④的化学方程式为 。
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图所示)。重复操作2-3次。写出铜丝由黑色变红的反应的化学方程式 。
(4)D与碳酸氢钠溶液反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列不属于配合物的是( )
A.[Cu(H2O)4]SO4·H2O B.[Ag(NH3)2]OH
C.KAl(SO4)2·12H2O D.Na3[AlF6]
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施对增大反应速率明显有效的是( )
A、Na与水反应时增大水的用量 B、Fe与稀硫酸反应制取氢气时,改用浓硫酸
C、在H2SO4与Na2CO3两溶液反应时,增大压强 D、反应N2+3H2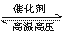 2NH3恒容增加氮气
2NH3恒容增加氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.增大压强,活化分子数增加,化学反应速率一定增大
B.升高温度,活化分子百分数增加,化学反应速率一定增大
C.活化分子间所发生的分子间的碰撞为有效碰撞
D.增大反应物浓度,使活化分子百分数增加,化学反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
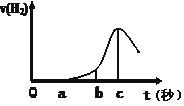 某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500 mL 0.5 mol·L-1的硫酸溶液中,右图为反应产生氢气速率与反应时间的关系图。
某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500 mL 0.5 mol·L-1的硫酸溶液中,右图为反应产生氢气速率与反应时间的关系图。
(1)关于图像的描述不正确的是 (填序号,下同);
① o→a段不产生产生H2是室温过低,反应难以发生。
② b → c段产生H2较快可能是反应放热,温度升高,加快了反应
③ c以后,产生H2速率逐渐下降原因可能是铝片趋于消耗完全
(2)在b到c这段时间内,收集到氢气VL(标准状况),则这段时间内用硫酸表示的平均速率为 mol/(L·s)(假设反应前后溶液体积不变)。
(3)其他条件不变,现换用500 mL 1 mol·L-1盐酸,产生氢气速率普遍较使用500 mL 0.5 mol·L-1硫酸的快,可能的原因是________;
(4)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,合理的有
①加入2 mol·L-1硝酸②加入少量CuSO4溶液 ③将铝片换成铝粉 ④增加硫酸的浓度至18 mol/L ⑤加CH3COONa固体; ⑥加入少量Na2SO4溶液
(5)催化剂会影响反应速率,请根据①反应写出FeCl3催化H2O2分解的另一反应原理(用离子方程式)①2Fe3++ H2O2= 2Fe2++ 2H+ +O2↑;② ;
查看答案和解析>>
科目:高中化学 来源: 题型:
硒(Se)是人体必需的微量元素,在元素周期表中的位置如下图。下列关于硒元素的叙述正确的是
| O | |
| S | |
| Se | Br |
A. 硒位于元素周期表第四周期第IVA族
B. 硒的非金属性比S弱
C. H2Se比HBr稳定
D. 最高价氧化物的化学式为SeO2
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如下,下列说法不正确的是 ( )
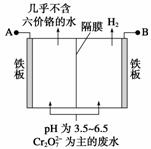
A.A为电源正极
B.阳极区溶液中发生的氧化还原反应为
Cr2O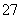 +6Fe2++14H+===2Cr3++6Fe3+
+6Fe2++14H+===2Cr3++6Fe3+ +7H2O
+7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O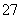 被还原
被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com