
【题目】前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是_________(填元素符号,下同)。
(2)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式_________,黄血盐晶体中各种微粒间的作用力不涉及______________(填序号)。
a.金属键 b.共价键 c.配位键
d.离子键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为___________________,很多不饱和有机物在E催化下可与H2发生加成:如①CH2=CH2 ②HC≡CH ③![]() ④HCHO。其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为______________,它加成后产物甲醇的熔、沸点比CH4的熔、沸点高,其主要原因是____________。
④HCHO。其中碳原子采取sp2杂化的分子有____________(填物质序号),HCHO分子的立体结构为______________,它加成后产物甲醇的熔、沸点比CH4的熔、沸点高,其主要原因是____________。
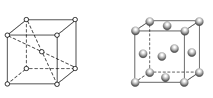
(4)金属C、F晶体的晶胞如下图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为_________。金属F的晶胞中,若设其原子半径为r,晶胞的边长为a,根据硬球接触模型,则r = _______a,列式表示F原子在晶胞中的空间占有率______________(不要求计算结果)。
【答案】K K4Fe(CN)6 aef 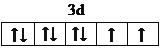 ①③④ 平面三角形 CH3OH分子之间存在氢键,熔、沸点比CH4高 2∶3
①③④ 平面三角形 CH3OH分子之间存在氢键,熔、沸点比CH4高 2∶3 ![]() a
a ![]() π×100%
π×100%
【解析】
前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,则A为碳元素、B为N元素;C、D、E、F是位于同一周期的金属元素,只能处于第四周期,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,可推知C为K、F为Cu,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2,D、E价电子排布分别为3d64s2,3d84s2,故D为Fe、E为Ni,据此分析解答。
根据上述分析,A为C元素,B为N元素,C为K元素,D为Fe元素,E为Ni元素,F为Cu元素。
(1)六种元素中K的金属性最强,最容易失去电子,其第一电离能最小,故答案为:K;
(2)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],化学式为K4[Fe(CN)6],黄血盐晶体中含有离子键、配位键、共价键,没有金属键、氢键和分子间作用力,故答案为:K4Fe(CN)6;aef;
(3)镍为28号元素,Ni2+的价层电子排布式为3d8,故价电子排布图为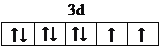 ;①CH2=CH2、③
;①CH2=CH2、③![]() 、④HCHO中C原子价层电子对数都是3,没有孤电子对,C原子采取sp2杂化;②HC≡CH为C原子价层电子对数是2,没有孤电子对,C原子采取sp杂化;HCHO分子的立体结构为平面三角形,它的加成产物为甲醇,甲醇分子之间能够形成氢键,其熔、沸点比CH4的熔、沸点高,故答案为:
、④HCHO中C原子价层电子对数都是3,没有孤电子对,C原子采取sp2杂化;②HC≡CH为C原子价层电子对数是2,没有孤电子对,C原子采取sp杂化;HCHO分子的立体结构为平面三角形,它的加成产物为甲醇,甲醇分子之间能够形成氢键,其熔、沸点比CH4的熔、沸点高,故答案为: ;①③④;平面三角形; CH3OH分子之间存在氢键,熔、沸点比CH4高;
;①③④;平面三角形; CH3OH分子之间存在氢键,熔、沸点比CH4高;
(4)金属K晶体为体心立方堆积,晶胞结构为左图,晶胞中K原子配位数为8,金属Cu晶体为面心立方最密堆积,晶胞结构为右图,以顶点Cu原子研究与之最近的原子位于面心,每个顶点Cu原子为12个面共用,晶胞中Cu原子配位数为12,K、Cu两种晶体晶胞中金属原子的配位数之比为 8∶12=2∶3;金属Cu的晶胞中,根据硬球接触模型的底面截面图为![]() ,则Cu原子半径为r和晶胞边长a的关系为:4r=
,则Cu原子半径为r和晶胞边长a的关系为:4r=![]() a,解得r=
a,解得r=![]() a;Cu原子数目=8×
a;Cu原子数目=8×![]() +6×
+6×![]() =4,4个Cu原子的体积为4×
=4,4个Cu原子的体积为4×![]() πr3=4×
πr3=4×![]() π×(
π×(![]() a)3,晶胞的体积为a3,Cu原子在晶胞中的空间占有率=
a)3,晶胞的体积为a3,Cu原子在晶胞中的空间占有率= =4×
=4×![]() π×(
π×(![]() )3×100%=
)3×100%=![]() π×100%,故答案为:2∶3;
π×100%,故答案为:2∶3;![]() a;
a;![]() π×100%。
π×100%。


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中有关物质的量浓度关系正确的是( )
A. 0.1 mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
B. NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)
C. 室温下,由pH=1的CH3COOH溶液与pH=13的NaOH溶液等体积混合,溶液中离子浓度大小的顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D. 常温下,在pH=8的NaA溶液中:c(Na+)-c(A-)=9.9×10-7 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH3COONa溶液中存在水解平衡:CH3COO-+H2O![]() CH3COOH+OH-,下列说法正确的是
CH3COOH+OH-,下列说法正确的是
A. 加入少量NaOH固体,c(CH3COO-)减小
B. 加入少量FeCl3固体,c(CH3COO-)减小
C. 稀释溶液,溶液的pH增大
D. 加入适量醋酸得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下几种有机物:
①CH4 ②CH3CH2OH ③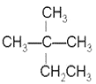 ④癸烷 ⑤CH3COOH ⑥
④癸烷 ⑤CH3COOH ⑥![]() ⑦
⑦![]() ⑧丙烷
⑧丙烷
请利用上述给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃的结构简式为______________;
(2)分子中含有14个氢原子的烷烃的分子式是__________;
(3)用“>”表示①③④⑧熔沸点高低顺序:_________________(填序号);
(4)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是______(填序号)
(5)有机物⑤和②在一定条件下发生反应的化学方程式是______________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇![]() 是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备
是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备![]() 的反应:
的反应:![]() ,在体积为1L的恒容密闭容器中,充2molCO和
,在体积为1L的恒容密闭容器中,充2molCO和![]() ,一定条件下发生上述反应,测得
,一定条件下发生上述反应,测得![]() 和
和![]() 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
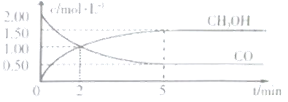
①从反应开始到5min,用一氧化碳表示的平均反应速率υ(CO)=______。
②下列说法正确的是______。
A.达到平衡时,![]() 的转化率为
的转化率为![]()
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氨气,反应速率减小
D.2min前υ(正)>υ(逆),2min后υ(正)<υ(逆)
(2)一定温度下,将![]() 与
与![]() 以体积比1:2置于密闭容器中发生反应:
以体积比1:2置于密闭容器中发生反应:
![]() ,达到平衡时
,达到平衡时![]() 的体积分数为
的体积分数为![]() ,该反应的平衡常数
,该反应的平衡常数![]() ______。
______。
(3)碳与水蒸气反应制取![]() 的相关反应如下:
的相关反应如下:
Ⅰ![]()
Ⅱ![]()
Ⅲ![]()
①计算反应![]() 的
的![]() ______
______![]()
②对于可逆反应![]() ,采取以下措施可以提高
,采取以下措施可以提高![]() 产率的是______。
产率的是______。
A.降低体系的温度
B.压缩容器的体积
C.增加CaO的量
D.选用适当的催化剂
(4)以甲醇为燃料,![]() 为氧化剂,KOH溶液为电解质溶液,可制成燃料电池
为氧化剂,KOH溶液为电解质溶液,可制成燃料电池![]() 电极材料为惰性电极
电极材料为惰性电极![]() 。若KOH溶液足量,写出此燃料电池负极的电极反应式:______;
。若KOH溶液足量,写出此燃料电池负极的电极反应式:______;
(5)若往20mL![]() 的弱酸
的弱酸![]() 溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是______
溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是______
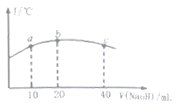
①该烧碱溶液的浓度为![]()
②该烧碱溶液的浓度为![]()
③![]() 的电离平衡常数:b点
的电离平衡常数:b点![]() 点
点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每天早上5:30起床学习化学会使人变得更加可爱聪明美丽帅气,而丑陋的人则会被尿憋醒,尿的主要成分是尿素,化学式为CO(NH2)2,结构可表示为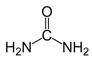 下列有关说法正确的是
下列有关说法正确的是
A.1mol CO(NH2)2分子中含有3mol δ键
B. CO(NH2)2分子中C原子、N原子的轨道杂化类型是均为sp3
C.组成尿素的四种元素第一电离能由大到小的顺序是O、N、C、H
D.根据结构推测,尿素可能易溶于水,熔沸点高于丙酮![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项比较中前者高于(或大于或强于)后者的是
A. 金属Mg和金属Cu的空间利用率
B. BF3和CH4中心原子的价层电子对数
C. 邻羟基苯甲醛(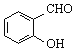 )和对羟基苯甲醛(
)和对羟基苯甲醛(![]() )的沸点
)的沸点
D. C-O和Si-O的键能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境保护是现代的世界性课题,人类已在多方面取得了突破性进展。
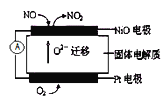
(1)连续自动监测氮氧化物![]() 的仪器--动态库仑仪已获得实际应用.它的工作原理如下图所示,NiO电极上NO发生的电极反应式为 ______。
的仪器--动态库仑仪已获得实际应用.它的工作原理如下图所示,NiO电极上NO发生的电极反应式为 ______。
(2)使用稀土催化剂有效消除汽车尾气中的![]() 、碳氢化合物也已逐渐成为成熟技术.压缩天然气汽车利用这一技术将
、碳氢化合物也已逐渐成为成熟技术.压缩天然气汽车利用这一技术将![]() 、
、![]() 转化成无毒物质,相关反应为:
转化成无毒物质,相关反应为:
①![]()
②![]()
③![]()
则![]() ______(用
______(用![]() 和
和![]() 表示)。
表示)。
(3)实验室在恒压下,将![]() 和
和![]() 置于密闭容器中发生反应③,测得在不同温度、不同投料比时,
置于密闭容器中发生反应③,测得在不同温度、不同投料比时,![]() 的平衡转化率如下表:
的平衡转化率如下表:
投料比 | 400K | 500K | 600K |
1 |
|
|
|
2 |
|
|
|
①在![]() 与
与![]() 反应时,可提高
反应时,可提高![]() 转化率的措施有 ______填编号
转化率的措施有 ______填编号![]() 。
。
A 增加催化剂的表面积 ![]() 改用高效催化剂
改用高效催化剂 ![]() 降低温度
降低温度
D 增大压强 ![]() 分离出
分离出![]()
![]() 减小
减小![]()
②![]() 时,将投料比为1的
时,将投料比为1的![]() 和
和![]() 的混合气体共
的混合气体共![]() ,充入容积为2L的装有催化剂的密闭容器中,反应经过5min达到平衡,试计算反应在该温度时的平衡常数______。(写出计算过程,计算结果保留三位有效数字)
,充入容积为2L的装有催化剂的密闭容器中,反应经过5min达到平衡,试计算反应在该温度时的平衡常数______。(写出计算过程,计算结果保留三位有效数字)
③若温度不变,在反应进行到10min时将容器的容积快速压缩为1L,请在答题卷表格中画出![]() 内,容器中
内,容器中![]() 物质的量浓度c随时间变化的曲线图______。
物质的量浓度c随时间变化的曲线图______。
(4)SNCR是一种新型的烟气脱氮环保技术,在有氧条件下,其脱氮原理是:![]() 和
和![]() 在
在![]() 催化剂表面的反应随温度的变化曲线如图所示,图中曲线表明,随着反应温度的升高,在有氧的条件下NO的转化率有一明显的下降过程,其原因可能是
催化剂表面的反应随温度的变化曲线如图所示,图中曲线表明,随着反应温度的升高,在有氧的条件下NO的转化率有一明显的下降过程,其原因可能是![]() 回答两条
回答两条![]() : ______。
: ______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.反应CaCO3(s)=CaO(s)+CO2(g),在常温下不能自发进行,则该反应的△H<0
B.0.lmol·L一1CH3COOH溶液加水稀释后,溶液中 的值减小
的值减小
C.铅蓄电池在放电过程中,负极质量增加,正极质量减少
D.锅炉中沉积的CaSO4和BaSO4都可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com