
���� ��1�������Ȼ�ѧ����ʽ��ϸ�˹���ɼ�������õ��Ȼ�ѧ����ʽ��Ȼ������ų������������ݷ�Ӧǰ��Ԫ�ػ��ϼ۱仯��������������ԭ��Ӧ�ĵ���ת�ƣ�
��2��ƫ�������ڵ�ȼ����������������������Ӧ�����ɵ�����ˮ�Ͷ�����̼��
��3��KOH��ҺΪ���Һ������ȼ�ϵ���У�ͨ��������һ��Ϊ��صĸ���������������Ӧ��
��4������Na2O2�������̼��ˮ������Ӧ����������ԭ�����Դ����ɴ���ռ�վ�������³´�л�����ġ���������
��� �⣺��1��6.4gҺ̬�����ʵ���=$\frac{6.4g}{32g/mol}$=0.2mol���ɸ�˹���ɿ�֪��Һ̬����������ⷴӦ���ɵ�����Һ̬ˮ���Ȼ�ѧ����ʽ��N2H4��l��+2H2O2��l���TN2��g��+4H2O��l����H=-817.6 kJ•mol-1����0.2 molҺ̬�·ų�������Ϊ0.2 mol��817.6 kJ/mol=163.5 kJ�����ݷ�Ӧǰ��Ԫ�ػ��ϼ۱仯��֪��N2H4��N2��4e-����6.4gҺ̬�����ʵ���Ϊ0.2mol�����ݵ����غ����õ�ת�Ƶ���Ϊ0.8mol��
�ʴ�Ϊ��0.8mol��163.5 kJ��
��2��ƫ�������ڵ�ȼ����������������������Ӧ�����ɵ�����ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��C2H8N2+2N2O4$\frac{\underline{\;��ȼ\;}}{\;}$3N2+4H2O+2CO2��
�ʴ�Ϊ��C2H8N2+2N2O4$\frac{\underline{\;��ȼ\;}}{\;}$3N2+4H2O+2CO2��
��3��KOH��ҺΪ���Һ������ȼ�ϵ���У�ͨ��������һ��Ϊ��صĸ���������������Ӧ���缫��ӦʽΪ��H2-2e-+2OH-=2H2O��
�ʴ�Ϊ��H2-2e-+2OH-=2H2O��
��4�����ݹ����������������̼��ˮ��Ӧ���������������˷ɴ���ռ�վ�������³´�л�����ġ�������������ʽΪ��2Na2O2+2CO2�T2Na2CO3+O2��2Na2O2+2H2O�T4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2CO2�T2Na2CO3+O2��2Na2O2+2H2O�T4NaOH+O2����
���� ������Ҫ�����Ȼ�ѧ����ʽ����д��������ԭ��Ӧ����ת�ơ�ԭ��صĹ���ԭ���ȣ���Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͶԻ���֪ʶ���ۺ�Ӧ��������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
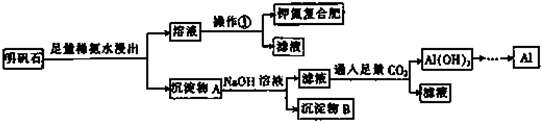
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ļ�ѧʽΪ��KAl��SO4��2 | |
| B�� | �����ӵĽṹʾ��ͼΪ��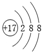 | |
| C�� | ����Ļ�ѧʽ��NaCO3 | |
| D�� | ��ˮ�ĵ��뷽��ʽ��NH3•H2O��NH4++H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 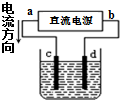 ������ͼʾװ�þ���ͭ����d��Ϊ��ͭ��c��Ϊ��ͭ���������ҺΪCuSO4��Һ | |
| B�� | 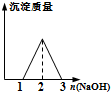 ������ʵ�����HCl��AlCl3��Һ�е���NaOH��Һ������ | |
| C�� |  �ﵽƽ��״̬��N2��g��+3H2��g��?2NH3��g����Ӧ����t1ʱ��С�������������t2ʱ�ִﵽƽ�� | |
| D�� | 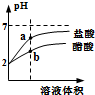 ��pH=2������ʹ���ֱ��ˮϡ�ͣ�a����Һ��ˮ�ĵ���̶ȱ�b����Һ��ˮ�ĵ���̶ȴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaClO3�ǻ�ԭ�� | |
| B�� | �����ԣ�ClO2��NaClO3 | |
| C�� | ��ѧ��Ӧ����ʽΪ��2NaClO3+Na2SO3+H2SO4=2ClO2+2Na2SO4+H2O | |
| D�� | 1 mol NaClO3�μӷ�Ӧ��2 mol e-ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ϸ�Ӧ | B�� | �ֽⷴӦ | C�� | �û���Ӧ | D�� | ���ֽⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƹ�ʹ�����ܡ�̫���ܣ����ٻ�ʯȼ�ϵ�ʹ�ã������ڼ������������ķ��� | |
| B�� | ��̫����ת��Ϊ�����Ǽ�����Ⱦ��������ԴΣ����һ�ֹ��� | |
| C�� | ʯ�͵ķ����ѻ����ѽ��ʯ�͵ļӹ���������Ŀ�ľ�Ϊ�õ���������� | |
| D�� | ú������Եõ�ú���ͣ�ú���ͽ�һ�������ֿɵõ������ױ����л��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com