
A.c(NO![]() )>c(OH-)>c(NH
)>c(OH-)>c(NH![]() )>c(Ba2+)
)>c(Ba2+)
B.c(NO![]() )> c(Ba2+)> c(OH-)>c(NH
)> c(Ba2+)> c(OH-)>c(NH![]() )
)
C.c(Ba2+)>
c(NO![]() )> c(OH-)>c(NH
)> c(OH-)>c(NH![]() )
)
D.c(NO![]() )> c(Ba2+)>c(NH
)> c(Ba2+)>c(NH![]() )> c(OH-)
)> c(OH-)
科目:高中化学 来源: 题型:013
将20 mL与0.4 mol•L-1硝酸铵溶液跟50 mL 0.1 mol•L-1氢氧化钡溶液混合,则混合溶液中各离子浓度的大小顺序是( )
A.c(NO![]() )>c(OH-)>c(NH
)>c(OH-)>c(NH![]() )>c(Ba2+)
)>c(Ba2+)
B.c(NO![]() )> c(Ba2+)> c(OH-)>c(NH
)> c(Ba2+)> c(OH-)>c(NH![]() )
)
C.c(Ba2+)>
c(NO![]() )> c(OH-)>c(NH
)> c(OH-)>c(NH![]() )
)
D.c(NO![]() )> c(Ba2+)>c(NH
)> c(Ba2+)>c(NH![]() )> c(OH-)
)> c(OH-)
查看答案和解析>>
科目:高中化学 来源:云南省昆明八中2012届高三上学期期中考试化学试题 题型:022
已知:①25℃时弱电解质的电离平衡常数:Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=1.5×10-10.②25℃时,2.0×10-3 mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
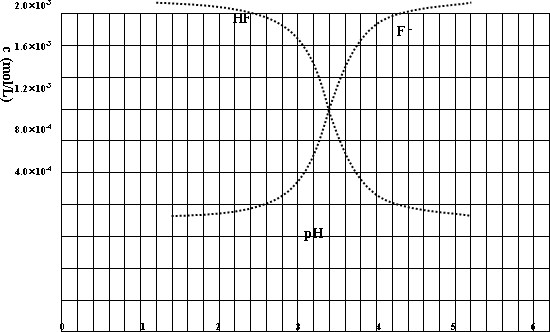
■(图有问题)
请根据信息回答下列问题:
(1)25℃时,将20 mL 0.10 mol·L-1 CH3COOH溶液和20 mL 0.10 mol·L-1 HSCN溶液分别与20 mL 0.10 mol·L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如下图:

反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是________,
反应结束后所得两溶液中,c(CH3COO-)________c(SCN-)(填“>”、“<”或“=”).
(2)25℃时,HF电离平衡常数的表达式Ka=________,25℃时,HF电离平衡常数Ka________.
(3)25℃时,将4.0×10-3 mol·L-1 HF溶液与4.0×10-4 mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省威海市高三上学期期末考试化学试卷(解析版) 题型:计算题
(1)已知25℃时有关弱酸的电离平衡常数:
|
弱酸化学式 |
HSCN |
CH3COOH |
HCN |
H2CO3 |
|
电离平衡常数 |
1.3×10—1 |
1.8×10—5 |
4.9×10—10 |
K1=4.3×10—7 K2=5.6×10—11 |
①等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为
(填序号)。
②25℃时,将20 mL 0.1 mol·L—1 CH3COOH溶液和20 mL 0.1 mol·L—1HSCN溶液分别与20 mL 0.1 mol·L—1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是 。反应结束后所得两溶液中,c(CH3COO—) c(SCN—)(填“>”、“<”或“=”)

③若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是______(填序号)。
a. c(CH3COO-) b. c(H+) c. Kw d. 醋酸电离平衡常数
(2)下图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2—浓度、金属阳离子浓度变化情况。如果向三种沉淀中加盐酸,最先溶解的是 (填化学式)。向新生成的ZnS浊液中滴入足量含相同浓度的Pb2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为 (填化学式)沉淀。

(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol·L—1的氯化铜溶液的装置示意图:

请回答:
① 甲烷燃料电池的负极反应式是 。
② 当线路中有0.1 mol电子通过时, 极增重________g
查看答案和解析>>
科目:高中化学 来源: 题型:
由周期表中前20号元素组成的单质X2、Y和化合物Z的有关信息如下表,X2、Y 和Z之间的转化关系如右图(其他无关物质已略去)。请回答下列问题:
| 元素X | 易形成-1价18电子的单核离子 |
| 元素Y | 第3周期第ⅥA族 |
| 化合物Z | 所含阳离子有3个电子层 |
| 常温下0.1 mol·L-1的水溶液pH=13 |
(1)用化学方程式表示X2在工业生产上的一种用途 。
(2) 比较元素X与Y的氢化物稳定性: 比 稳定(填氢化物化学式)。
(3)将0.24 mol Y氧化物YO2和 0.11 mol氧气放入容积为1 L的密闭容器中,一定条件下反应达到平衡,得到0.12 mol YO3气体,同时放出热量11.8kJ。
①该反应平衡常数= 。
②该反应的热化学方程式为 。
(4) C能与稀硫酸反应生成能使品红溶液褪色的气体,D中所含阴、阳离子的电子层排布相同。
①写出Y与Z反应的离子方程式
②将20 mL 0.5 mol·L-1 C溶液逐滴加入到V mL 0.2 mol·L-1 KMnO4溶液(硫酸酸化)中,溶液恰好褪色(此时Mn元素恰好变为Mn2+)。计算V= 。
(5)用石墨作电极,在隔膜电解槽中电解A的溶液,可制得Z的水溶液,请写出甲烷燃料电池(Z的水溶液为电解质溶液)负极的电极反应式
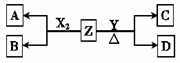
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com