
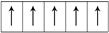
 ,而不排布成
,而不排布成 ,其最直接的根据是
,其最直接的根据是| A.能量最低原理 | B.泡利不相容原理 | C.原子轨道能级图 | D.洪特规则 |
科目:高中化学 来源:不详 题型:填空题
| 元素代号 | W | R | X | Y | Z |
| 原子半径/nm | 0.037 | 0.154 | 0.066 | 0.070 | 0.077 |
| 主要化合价 | +1 | +1 | -2 | -3、+5 | +2、+4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.杂化前后的轨道数不变,但轨道的形状发生了改变 |
| B.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180° |
| C.部分四面体形、三角锥形、V形分子的结构可以用sp3杂化轨道解释 |
| D.杂化轨道全部参加形成化学键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.13C与15N有相同的中子数 |
| B.13C与C60互为同素异形体 |
| C.15N与14N互为同位素 |
| D.15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氢化物稳定性增强:HF、H2O、NH3 | B.酸性减弱:HClO4、HBrO4、HIO4 |
| C.还原性增强:A1、Mg、Na | D.非金属性减弱:Cl、S、P |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10Be、9Be、8Be核内质子数均是4 |
| B.Be元素在元素周期表的p区 |
| C.氢核聚变后会产生新元素 |
| D.从矿物中提取单质铍的过程中铍一定被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳原子核外电子有六种运动状态 | B.NH4+中N原子轨道杂化类型为sp3 |
| C.电负性:O > Cl | D.第一电离能 Al > Mg |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.W、Y、Z的电负性大小顺序一定是Z>Y>W |
| B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C.Y、Z形成的分子的空间构型可能是正四面体 |
| D.WY2分子中σ键与π键的数目之比是2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com