
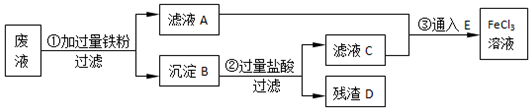
分析 由流程图可知废液的处理过程为:工业废液里含有FeCl2、CuCl2和FeCl3.用过量铁粉把生成的氯化铜置换得到金属铜,同时把过量的氯化铁溶液转变为氯化亚铁溶液,过滤所得沉淀B为铁和铜,用过量盐酸溶解铁后分离铜和铁,残渣D为Cu,最后,进行过滤分离出金属铜而回收铜,滤液C为氯化亚铁溶液,最后,进行过滤分离出金属铜而回收铜,并把滤液A和滤液C为氯化亚铁溶液合并,通入E为氯气,氯化亚铁与氯气反应而转化为氯化铁溶液循环利用.
解答 解:(1)反应后的滤液A为FeCl2,E为Cl2,故答案为:FeCl2;Cl2;
(2)CuCl2和FeCl3中加入铁粉,分别发生:Fe+2FeCl3=3FeCl2,Fe+CuCl2=Cu+FeCl2,B的化学成份为Fe、Cu,回收的铜是D,
故答案为:Fe、Cu;D;
(3)Fe比Cu活泼,可与盐酸反应生成而分离出Cu,反应②的化学方程式为:Fe+2HCl=FeCl2+H2↑,
故答案为:Fe+2HCl=FeCl2+H2↑.
点评 本题考查物质的分离,题目难度中等,注意根据流程结合物质的性质解答该题.


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠的摩尔质量是40 g | |
| B. | 1 mol NaOH的质量是40 g/mol | |
| C. | 1gH2和lgN2含分子数相等 | |
| D. | 等质量的N2、CH4、CO、H2O中,CH4含分子数最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| X | Y | |
| Z | W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
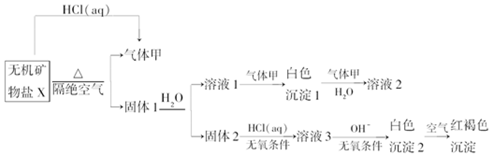
 ,写出气体甲的电子式
,写出气体甲的电子式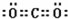 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c.则a、b、c分别为( )
分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c.则a、b、c分别为( )| A. | 4、4、7 | B. | 4、3、6 | C. | 3、5、4 | D. | 2、6、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
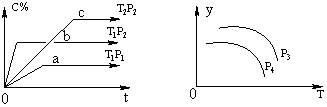
| A. | p3>p4,y轴表示A的物质的量分数 | |
| B. | 若增大A的浓度,平衡体系颜色加深,C一定是有颜色的气体 | |
| C. | p3<p4,y轴表示平衡常数K | |
| D. | p3>p4,y轴表示混合气体的平均摩尔质量 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.含有 NA个氦原子的氦气在标准状况下的体积约为11.2L
B.25℃,1.01×105Pa,64g SO2中含有的原子数为3NA
C.在常温常压下,11.2L Cl2含有的分子数为0.5NA
D.在标准状况下,11.2L H2O含有的分子数为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com