
【题目】A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍。A的一种原子中,质量数与质子数之差为零。D元素原子的最外层电子数为m,次外层电子数为n。E元素原子的L层上电子数为(m+n),M层上电子数为![]() 。请回答下列问题:
。请回答下列问题:
(1)B元素是________,D元素在周期表中的位置是________。
(2)C与E形成的化合物E3C属于________(填“原子”“离子”或“分子”)晶体。
(3)由A、D、E元素组成的化合物中存在的化学键类型是________。
(4)写出一个E和D形成的化合物与水反应的离子方程式:_________________________。
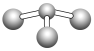
(5)已知:甲+H2O→丙+丁,该反应不是氧化还原反应。若甲是由N和Cl元素组成的化合物,其分子结构模型如下图所示,丙具有漂白性。丁与H2O有相同的电子总数,则丁的电子式为_________________。
(6)与D同主族且上下相邻的元素M、N,原子电子层数M>N>D,三种元素的氢化物的稳定性由大到小的顺序是________________________(填化学式)。
【答案】C(或碳) 第2周期ⅥA族 离子 离子键和共价键 Na2O+H2O===2Na++2OH-(或2Na2O2+2H2O===4Na++4OH-+O2↑) ![]() H2O>H2Se>H2S
H2O>H2Se>H2S
【解析】
A、B、C、D、E五种短周期元素,B原子的最外层电子数是其次外层电子数的2倍,B原子只能有2个电子层,最外层电子数为4,则B为碳元素;A的一种原子中质量数与质子数之差为零,即没有中子,则A为氢元素;D元素的原子最外层电子数为m,次外层电子数为n,E元素的原子L层电子数为m+n,M层电子数为m/2-n,则m+n=8,m<8,所以n=2,则m=8-2=6, D为氧元素;因为原子序数依次增大,所以C是氮元素;E的M层电子数=6/2-2=1,所以E为Na;所以A、B、C、D、E五种短周期元素分别是H、C、N、O、Na,以此解答该题。
(1)根据分析,B元素是碳,D元素是氧,氧元素在周期表中的位置是:第2周期ⅥA族,正确答案:碳(C);第2周期ⅥA族;
(2)C元素是N,E元素是Na,形成的化合物是Na3N,是离子化合物,属于离子晶体,正确答案:离子晶体;
(3)由A、D、E元素组成的化合物是NaOH,NaOH中存在的化学键类型是:共价键和离子键,正确答案:离子键、共价键;
(4)E和D形成的化合物为氧化钠或过氧化钠,与水反应的离子方程式为:Na2O+H2O=2Na++2OH或2Na2O2+2H2O=4Na++4OH+O2↑,故答案为:Na2O+H2O=2Na++2OH或2Na2O2+2H2O=4Na++4OH+O2↑;
(5)若甲是由N和Cl元素组成的化合物,其分子结构模型如图所示,根据其模型知,大球是Cl原子,小球是N原子,所以该物质是NCl3,丙具有漂白性,根据元素守恒知,丙是次氯酸,因为该反应是非氧化还原反应,Cl元素的化合价不变,所以甲中氯元素的化合价是+1价,丁与H2O有相同的电子总数,结合原子守恒知,丁是NH3,丁的电子式为:![]() ,正确答案:
,正确答案:![]() ;
;
(6)与D同主族上下相邻的元素M、N,原子电子层数M>N>D,则M为Se、N为S,水分子之间存在氢键,沸点最高,H2S与H2Se结构组成形式,H2Se相对分子质量较大,分子间作用力较强,H2Se沸点较H2S高,所以沸点H2O>H2Se>H2S,正确答案为:H2O>H2Se>H2S。


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】节约资源、保护环境,共同守护我们赖以生存的地球是每个人的责任。下列做法值得提倡的是
A.大力开采化石燃料
B.交通出行优先使用私家车
C.超市购物使用一次性塑料袋
D.回收利用垃圾中的有用资源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小粒钠投入盛有硫酸铜溶液的小烧杯中,不可能观察到的现象是( )
A. 溶液中出现蓝色絮状沉淀 B. 有红色的铜被置换出来
C. 钠粒熔成小球浮在水面四处游动 D. 有气体产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸通常以二水合物的形式存在,俗称草酸晶体.已知草酸晶体在101℃时熔化并开始升华,157℃时大量升华,继续升温会分解生成CO、CO2和H2O。
(1)下列关于乙二酸的叙述正确的是(填编号)_____________
①能和乙二醇发生酯化反应
②能使酸性高锰酸钾溶液褪色
③其溶液能使蓝色石蕊试纸变红
④能和碳酸氢钠溶液反应生成气体
(2)乙二酸的工业生产方法之一是以乙二醇为原料,在一定条件下,用空气氧化得到.写出该反应的化学反应方程式:__________________________________
(3)欲检验草酸晶体受热分解的产物中是否有CO2,甲、乙两位同学分别设计了装置1、装置2来完成实验.
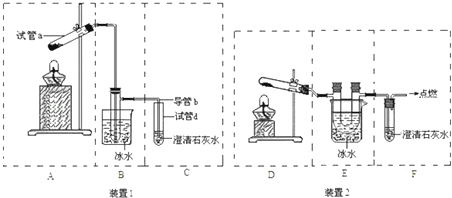
(Ⅰ)简述检验装置1气密性的操作方法:______________________________________
(Ⅱ)B和E两个装置中更合理的是______________
(Ⅲ)请从A~F中选择合适的仪器,组装一套可更好达到实验目的装置,按照气流由左到右的顺序依次为(用字母表示):________________.
(Ⅳ)一定条件下草酸氢铵分解生成NH3、CO、CO2和H2O,110℃时将该混合气体先通过Na2O2,再通过浓硫酸分别增重Ag和Bg; 若将混合气体先通过浓硫酸,再通过Na2O2分别增重Cg和Dg(能反应的气体均可吸收完全,且该条件下CO与Na2O2不反应),则A、B、C、D的大小关系为:______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是( )
2Z(g),此反应达到平衡的标志是( )
A. 单位时间内消耗0.1 mol X的同时生成0.2 mol Z
B. v正(X) =v逆(Z)
C. 容器内X、Y、Z的浓度之比为1∶2∶2
D. 容器内压强不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 (1)如图所示,若溶液C为浓硝酸,电流表指针发生偏转,B电极材料为Fe,A电极材料为Cu,则B电极的电极反应式为_________,A电极的电极反应式为____________;反应进行一段时间后溶液C的酸性会____(填“增强”“减弱”或“基本不变”)。
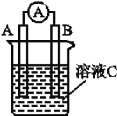
(2)我国首创以铝—空气—海水电池作为能源的新型海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是______(填化学名称),负极反应为___________;正极反应为_________。
(3)熔融盐电池具有高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,其负极反应式为2CO+2CO32---4e-![]() 4CO2,则正极反应式为_____,电池总反应式为______。
4CO2,则正极反应式为_____,电池总反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为元素周期表中前三周期的主族元素,它们的原子序数按A、B、C、D、E的顺序增大。A的最外层电子数是次外层电子数的2倍,C与E最外层电子数相等,E的最高价氧化物中含氧60%,D与C可形成D2C、D2C2两种离子化合物。填写下列空白:
(1)写出上述五种元素的元素符号:A___,B___,C___,D____,E___。
(2)写出D2C2的电子式_________,AC2的结构式___________。
(3)用电子式表示 AC2化合物的形成过程__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com