


| 8.34g |
| 278g/mol |
| ||
| ||
| ||
| wg |
| 233g/mol |
| 2W |
| 233g/mol |
| 2W |
| 233g/mol |
| W×152×2 |
| 233 |
| W×152×2 |
| 233 |


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
| ||
A、有
| ||
B、有
| ||
C、有
| ||
D、有
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、粗铜接电源负极 |
| B、精铜作阴极 |
| C、杂质都将以单质形式沉积到池底 |
| D、精铜片增重2.56g,电路中通过电子为0.04mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
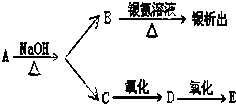 有机物A、B、C、D、E有如下衍生关系,又知C和E在浓H2SO4作用下加热,得到一种具有果香味的液体,分子式为C4H8O2.试写出A、B、C、D、E的结构简式.
有机物A、B、C、D、E有如下衍生关系,又知C和E在浓H2SO4作用下加热,得到一种具有果香味的液体,分子式为C4H8O2.试写出A、B、C、D、E的结构简式.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、同等条件下,正丁腈在水中的溶解度比在乙醚中的溶解度大 |
| B、其分子式为C4H7N,其密度比水大 |
| C、它还可被命名为氰代丙烷,正丙基氰等,其结构中不含氢键 |
| D、正丁腈由丁烯与氨氧化而得,或由丁醇与氨催化氧化而得 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com