
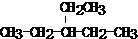
分析 (1)①选取含羟基碳在内的最长碳链为主碳链,从离羟基近的一端编号,先判断官能团及其位置,再命名;
②烷烃中含有取代基乙基,则主链至少含有5个C原子,据此写出满足条件的烷烃的结构简式;
(2)①依据结构式命名即可,选取最长碳链为主链,从离支链近的一端编号,书写名称;
②根据加成原理采取逆推法还原C=C双键,烷烃分子中相邻碳原子上均带氢原子的碳原子间是对应烯烃存在碳碳双键的位置.还原双键时注意:先判断该烃结构是否对称,如果对称,只考虑该分子一边的结构和对称线两边相邻碳原子即可;如果不对称,要全部考虑,然后各去掉相邻碳原子上的一个氢原子形成双键;原来烯烃的同分异构体中有一种的核磁共振氢谱有两个峰,且比例为1:3,则氢原子有两种为2个和6个,据此书写结构简式;
解答 解:(1)①CH3CH(CH3)CH2CH2OH,主链碳原子数为4,1号位含有一个-OH,3号位含有一个甲基,其名称为:3-甲基-1-丁醇,
故答案为:3-甲基-1-丁醇;
②乙基至少在3号位,只有一个乙基,则主链最少含有5个C,则式量最小的烷烃的结构简式为: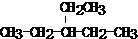 ,
,
故答案为: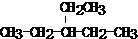 ;
;
(2)①CH3-CH(CH3)2正确命名为,主链为3个,甲基在第二个碳原子,得到名称为:2-甲基丙烷,故答案为:2-甲基丙烷;
②根据烯烃与H2加成反应的原理,推知该烷烃分子中相邻碳原子上均带氢原子的碳原子间是对应烯烃存在碳碳双键的位置,因此相应烯烃分子中存在碳碳双键的位置只有1种,结构简式为:CH2=C(CH3)2,原来烯烃的同分异构体中有一种的核磁共振氢谱有两个峰,且比例为1:3,则氢原子有两种为2个和6个,据此书写结构简式为:CH3-CH=CH-CH3,
故答案为:CH2=C(CH3)2;CH3-CH=CH-CH3
点评 本题考查了化学反应过程分析判断,同分异构体书写,理解加成反应原理是解题的关键,采取逆推法还原C=C双键,注意分析分子结构是否对称,防止重写、漏写,题目难度不大.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:解答题
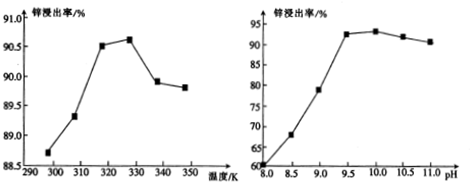
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正、逆反应速率相等均为零 | |
| B. | 反应物和生成物的浓度保持一定 | |
| C. | SO2、O2、SO3分子数目之比为2:1:2 | |
| D. | 单位时间内消耗a mol SO2,同时生成a mol SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 提倡低碳生活 | B. | 大力发展私家车,减少公共交通 | ||
| C. | 利用太阳能、风能等代替化石能源 | D. | 多利用电动车和自行车 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
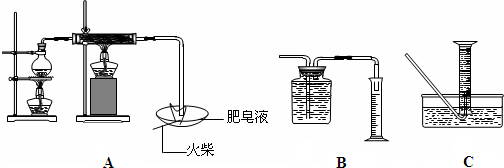
| 现象 | 结论与解释 | |
| 可能① | ||
| 可能② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C原子外围电子排布图: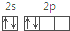 | B. | 硫原子结构示意图: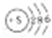 | ||
| C. | 二氧化硅的分子式:SiO2 | D. | 苯的比例模型: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com