

 )是味精的主要成分.当前我国生产味精主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖.
)是味精的主要成分.当前我国生产味精主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖. 可知,离子(1)的结构简式是
可知,离子(1)的结构简式是 ,故答案为:
,故答案为: ;
;| 催化剂 |
| △ |
| 催化剂 |
| △ |
| (c1V1-C 2V 2)×10 -3mol×58.5g/mol |
| mg |
| 5.85(c 1V 1-c 2V 2) |
| m |
| 5.85(c 1V 1-c 2V 2) |
| m |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、向足量的NaHS 溶液中通入少量氯气:HS-+Cl2=S↓+H++2Cl- |
| B、碳酸钡溶于醋酸:BaCO3+2H+=Ba2++H2O+CO2↑ |
| C、饱和的Na2CO3溶液中通CO2气体:2Na++CO32-+H2O+CO2=2NaHCO3↓ |
D、把水杨酸( )加到足量的Na2C03溶液中: )加到足量的Na2C03溶液中: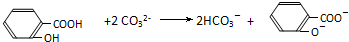 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D均为中学化学常见的物质,其组成元素均为主族元素.它们间的反应关系如下图所示.(除(2)外,反应均在常温下进行)
A、B、C、D均为中学化学常见的物质,其组成元素均为主族元素.它们间的反应关系如下图所示.(除(2)外,反应均在常温下进行)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相同质量的水和冰相比较,冰的能量高 |
| B、化学反应过程中能量的变化只有吸热和放热两种表现形式 |
| C、化学反应既遵循质量守恒,也遵循能量守恒 |
| D、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m>n | B、m<n |
| C、m=n | D、不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蛋白质溶液中加入饱和的硫酸铵溶液,蛋白质析出,如再加水能溶解 |
| B、蛋白质中的蛋白质分子能透过滤纸,但不能透过半透膜 |
| C、重金属盐能使蛋白质变性,所以吞服“钡餐”会引起中毒 |
| D、浓硝酸溅在皮肤上,能使皮肤呈黄色是由于蛋白质与浓硝酸发生了颜色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、放电时的正极反应为O2+2H2O+4e-═4OH- |
| B、充电时正极附近pH降低 |
| C、若用该电池作电源电解硫酸镁溶液,当电路中有0.02转移时,阴极增重0.24g |
| D、在该电池中,放电反应生成的不是固体的Li2O,而是容易溶解在水性电解液中的LiOH (氢氧化锂).因此,氧化锂在空气电极堆积后,不会导致工作停止 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com