
【题目】甲苯是由苯环和甲基结合而成的,甲苯能够使酸性KMnO4溶液褪色是因为
A. 烷烃能使酸性KMnO4溶液褪色B. 苯环能使酸性KMnO4溶液褪色
C. 苯环使甲基的活性增强而导致的D. 甲基使苯环的活性增强而导致的
科目:高中化学 来源: 题型:
【题目】下列几种氢键:①O—H…O,②N—H…N,③F—H…F,④O—H…N,按氢键从强到弱的顺序正确的是 ( )
A.③>①>④>② B.①>②>③>④
C.③>②>①>④ D.①>④>③>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鲍林被认为是20世纪对化学科学影响最大的人之一,他也是两位获得诺贝尔奖不同奖项的人之一。杂化轨道是鲍林为了解释分子的立体构型提出的,下列对sp3、sp2、sp杂化轨道的夹角的比较,得出结论正确的是( )
A.sp杂化轨道的夹角最大
B.sp2杂化轨道的夹角最大
C.sp3杂化轨道的夹角最大
D.sp3、sp2、sp杂化轨道的夹角相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组探究Fe3+和SO![]() 之间发生的反应。
之间发生的反应。
(1)取5 mL FeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。无气泡产生,无沉淀生成。这种红褐色液体是_________。
(2)除了观察到以上的现象外,有成员提出了另一种可能:发生氧化还原反应。反应的离子方程式为________________________。
(3)研究性学习小组设计了两种实验方案证明发生了氧化还原反应。请把实验方案补充完整:
(方案一)检验溶液中含有Fe2+证明发生了氧化还原反应
(方案二)检验溶液中含有____证明发生了氧化还原反应
实验用品:0.1 mol·L-1 BaCl2、3 mol·L-1 盐酸、3 mol·L-1 硝酸、新制氯水、20% KSCN、0.5 mol·L-1 KI;试管若干、胶头滴管若干。
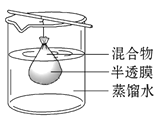
Ⅰ.预处理:将(1)中获得的混合物放在如图装置中处理足够时间,该操作名称为____。
Ⅱ.检验过程
①简述证明溶液中含有Fe2+的操作方法:_________________________________________;
②检验溶液中含有另一种离子可选用的试剂是:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行化学实验必须注意安全,下列操作不正确的是
A.点燃氢气前要检验氢气的纯度,以免发生爆炸
B.用酒精灯内焰加热试管,加热试管前可以不预热试管
C.CO气体有毒,处理CO尾气时可将其点燃,转化为无毒的CO2
D.不慎将水银洒落在地面上,应立即用硫粉覆盖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将红热的固体单质M放入浓硝酸中,剧烈反应,产生混合气体A,A在常温下不与空气接触时,发生如图所示的变化。

(1)混合气体A的主要成分是____________。
(2)气体B为__________,蓝色溶液D为____________。
(3)单质M与浓硝酸反应的化学方程式是____________________________。
(4)单质C与稀硝酸反应的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是
A.Ag+、 K+、 NO3-、 Cl-B.Mg2+、 Na+、 Cl-、 SO42-
C.NH4+、 Mg2+、 OH-、 Cl-D.H+、 Na+、 CO32-、 SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.1mol氯含有6.02×1023个微粒
B.阿伏加德罗常数的数值约等于6.02×1023
C.钠的摩尔质量就是它的相对原子质量
D.标准状况下,1 mol任何物质体积均为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)中国古代四大发明之一一黑火火药,它的爆炸反应为;S+2KNO3+3C ![]() 3CO2↑+A+N2↑(已配平)
3CO2↑+A+N2↑(已配平)
①除S外,上列元素的电负性从大到小依次为______.
②在生成物中,A的晶体类型为_______,含极性共价键的分子的中心原子轨道杂化类型为_______.
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为_________.
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为______,Q2+的未成对电子数是________.
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)]6-nx+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)]6-nx++xR-H→Rx[CrCln(H2O)]6-n+xH+交换出来的H+经中和测定,即可求出x和n,确定配离子的组成。将含0.0015mol[CrCln(H2O)]6-nx+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200molL-1NaOH溶液25.00mL,该配离子的化学式为______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com