
NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.5.6g铁与足从稀盐酸反应.转移0.3NA个电子
B.10LpH=1的硫酸溶液中,所含的H+数为NA
C.1L1mol/L的醋酸钠溶液中,所含的CH3COO-数目等于NA
D.28gC2H4和C3H6的混合气体中碳原子数为NA
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源:2017届重庆市高三上定时训练(七)化学试卷(解析版) 题型:选择题
20.14g铜金合金与足量的某浓度HNO3反应,将产生的气体用1.12L(标准状况)O2混合,通入水中,气体恰好被完全吸收,则合金中铜的质量为
A.9.6g B.6.4g C.3.2g D.1.6g
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
一种可充电电池镍氢电池在放电过程中的总反应方程式是:NiOOH+ MH =Ni(OH)2+ M(M位储氢材料)下列说法正确的是
A.NiMH 电池放电过程中,正极的电极反应式为:NiOOH + H2O + e-= Ni(OH)2 + OH-
B.充电过程中OH-离子从阳极向阴极迁移
C.充电过程中阴极的电极反应式:H2O + M + e-= MH+ OH-,H2O中的H被M还原
D.NiMH电池中可以HCl溶液作为电解质溶液
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上月考二化学试卷(解析版) 题型:选择题
用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是
①加盐酸溶解②加烧碱溶液溶解③过滤
④通入过量CO2生成Al(OH)3沉淀
⑤加入盐酸生成盐胜生成Al(OH)3沉淀
⑥加入过量烧碱溶液
A.①⑥⑤③ B.②③④③ C.②③⑤③ D.①③⑤③
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上月考二化学试卷(解析版) 题型:选择题
下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)

A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上学期10月月考化学试卷(解析版) 题型:填空题
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)检验FeCl3溶液中阳离子的方法是
(2)FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)
FeCl3溶液也常用于腐蚀印刷电路板,反应的离子方程式为
(3)通过控制条件,将FeCl3水解产物聚合,生成聚合氧化铁,离子方程式为:xFe3++yH2O 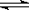 Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是 (填序号)。
Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是 (填序号)。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
(4)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3。完成NaClO3 氧化FeCl2 的离子方程式 。
(5)处理废水时,发现FeCl3并不能使酸性废水中的悬浮物沉降除去,其原因是______________。
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上学期10月月考化学试卷(解析版) 题型:选择题
化学与生活、生产密切相关,下列有关叙述正确的是
A.氢氧化铝、小苏打、纯碱均可用作胃酸中和剂
B.古代的陶瓷、水泥、石英玻璃等,都是硅酸盐产品
C.将草木灰(含K2CO3)与NH4Cl混合使用会降低肥效
D.石油的分馏、煤的干馏等物理变化在生产中有着重要的地位
查看答案和解析>>
科目:高中化学 来源:2017届河北邯郸市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列关于卤素的说法正确的是( )
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.氧化性Cl2>Br2>I2还原性Cl->Br->I-
C.实验室制备Cl2,可用排饱和食盐水集气法收集
D.氯水具有酸性,能使紫色石蕊试剂先变红后退色,也可用pH试纸测量其pH值。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三上学期10月月考化学试卷(解析版) 题型:填空题
碳、硫和氮元素及其化合物的处理,是资源利用和环境保护的重要研究课题。
⑴CO可转化成二甲醚,原理为:2CO(g) + 4H2(g)  CH3OCH3(g) + H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比的变化曲线如下图左所示,若温度升高,则反应的平衡常数K将 (填“增大”、“减小”或“不变”)
CH3OCH3(g) + H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比的变化曲线如下图左所示,若温度升高,则反应的平衡常数K将 (填“增大”、“减小”或“不变”)

⑵SO2的水溶液呈酸性,某温度下,0.02mol/L亚硫酸水溶液的pH等于2,若忽略亚硫酸的二级电离和H2O的电离,则该温度下亚硫酸的一级电离平衡常数Ka1= 。
⑶已知:反应1 2SO2(g) + O2(g)  2SO3(g) ΔH1
2SO3(g) ΔH1
反应2 2NO(g) + O2(g)  2NO2(g) ΔH2
2NO2(g) ΔH2
若ΔH1 <ΔH2 < 0,则反应3 SO2(g) + NO2(g)  SO3(g) + NO(g) 属于 (填“放热”或“吸热”)反应。
SO3(g) + NO(g) 属于 (填“放热”或“吸热”)反应。
⑷若用少量NaOH溶液吸收SO2气体,对产物NaHSO3进一步电解可制得硫酸,电解原理示意图(见上图右所示),则电解时阳极的电极反应式为 。
⑸在恒温密闭容器中通入SO2和NO2各1mol发生反应3:SO2(g) + NO2(g)  SO3(g)
SO3(g) + NO(g),当反应达到平衡后(此时NO2的转化率为α1),维持温度和容积不变,10min时再通入各1mol的SO2和NO2的混合气体,20min时再次平衡(此时NO2的转化率为α2)。两次平衡时NO2的转化率α1 α2(填“>”、“<”、“=”),并在下图中画出正反应速率在10-30min间随时间变化的曲线图。
+ NO(g),当反应达到平衡后(此时NO2的转化率为α1),维持温度和容积不变,10min时再通入各1mol的SO2和NO2的混合气体,20min时再次平衡(此时NO2的转化率为α2)。两次平衡时NO2的转化率α1 α2(填“>”、“<”、“=”),并在下图中画出正反应速率在10-30min间随时间变化的曲线图。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com