
 ,其余各能层电子全充满。
,其余各能层电子全充满。
 ;1s22s22p63s23p63d10;(2)平面三角形;
;1s22s22p63s23p63d10;(2)平面三角形;  NH3·HDO+D+。
NH3·HDO+D+。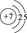 。Cu+离子的电子排布式为1s22s22p63s23p63d10;(2)SO2具有漂白性,该化合物分子中中心原子的VSEPR构型为平面三角形。(3)金属Al是由Al3+和自由电子构成的。当给某金属加热时,该区域的金属阳离子和自由电子的能量都增大,自由电子的质量小,惯性小,运动速度快,当其运动碰撞其它金属阳离子时,就把能量传递给该区域的金属,自由电子与金属铝离子频繁碰撞,形成热的传导;从而使整个金属的温度趋于一致,因此金属具有良好导热性。(4)元素的非金属性Cl>S。元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。所以E、F的最高价氧化物对应的水化物的酸性强弱顺序是HClO4>H2SO4;(5)一个晶胞中G的原子个数为8×1/8+6×1/2="4." (6)A与B形成的10电子阳离子为NH4+,在重水(D2O)中的水解离子方程式为NH4++D2O
。Cu+离子的电子排布式为1s22s22p63s23p63d10;(2)SO2具有漂白性,该化合物分子中中心原子的VSEPR构型为平面三角形。(3)金属Al是由Al3+和自由电子构成的。当给某金属加热时,该区域的金属阳离子和自由电子的能量都增大,自由电子的质量小,惯性小,运动速度快,当其运动碰撞其它金属阳离子时,就把能量传递给该区域的金属,自由电子与金属铝离子频繁碰撞,形成热的传导;从而使整个金属的温度趋于一致,因此金属具有良好导热性。(4)元素的非金属性Cl>S。元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。所以E、F的最高价氧化物对应的水化物的酸性强弱顺序是HClO4>H2SO4;(5)一个晶胞中G的原子个数为8×1/8+6×1/2="4." (6)A与B形成的10电子阳离子为NH4+,在重水(D2O)中的水解离子方程式为NH4++D2O NH3·HDO+D+;
NH3·HDO+D+;

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

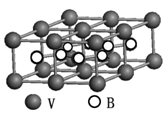
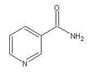
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
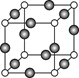
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
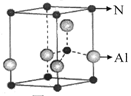


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | CH4 | SiH4 | NH3 | PH3 |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1 073 | 713.2 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | 0.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com