
| A | B | C | D | |
| 分子式 | C3H8O | C4H8Cl2 | C7H16 | C8H10 |
| 限定条件 | 能使KMnO4溶液褪色 | 分子中含有2个甲基 | 分子中含有3个甲基 | 芳香烃、能得到三种一硝基化物 |
| 数目 | 2 | 3 | 2 | 3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.C3H8O为饱和一元醇,能使KMnO4溶液褪色,说明与羟基相连的碳上有氢原子;
B.二氯代物的同分异构体可以采用“定一移二”法解题,先找出所有的同分异构体,再找出只含2个“-CH3”的;
C.可以根据有机物烷烃的同分异构体的写法来书写其所有的同分异构体,观察得出结论,还可以根据规律来推理获得答案;
D.芳香烃说明含有苯环,能得到三种一硝基化物说明苯环上有3种氢原子.
解答 解:A.C3H8O为饱和一元醇,能使KMnO4溶液褪色,说明与羟基相连的碳上有氢原子,可能为CH3CH2CH2OH、(CH3)2CHOH,故A正确;
B.C4H8Cl2的同分异构体可以采取“定一移二”法 ,由图可知C4H8Cl2共有9种同分异构体,其中图1中无论另一氯在什么位置,分子中都没有2个甲基,图2中另一氯在1、2号碳上,分子中含2个甲基,图3中另一氯在1、2号碳上,分子中含2个甲基,所以分子中含2个甲基的同分异构体有共4种,故B错误;
,由图可知C4H8Cl2共有9种同分异构体,其中图1中无论另一氯在什么位置,分子中都没有2个甲基,图2中另一氯在1、2号碳上,分子中含2个甲基,图3中另一氯在1、2号碳上,分子中含2个甲基,所以分子中含2个甲基的同分异构体有共4种,故B错误;
C.3个甲基需要一个支链是甲基,主链是己烷,左右各有一个-CH3,支链的甲基只能加在2或3号C上,4号C与3号C相同,5号C与2号C相同,还有一种是含有乙基的,即3-乙基戊烷,共三种,分别是2-甲基己烷、3-甲基己烷与3-乙基戊烷,故C错误;
D.芳香烃说明含有苯环,能得到三种一硝基化物说明苯环上有3种氢原子,分子式为C8H10的芳香烃,分子中含有1个苯环,故侧链为烷基,若有1个侧链,为-CH2-CH3,有一种;若有2个侧链,为-CH3,有邻、间、对三种,苯乙烷中,苯环上的一硝基代物有3种,邻二甲苯中,苯环上的一硝基代物有2种,间二甲苯中,苯环上的一硝基代物有3种,对二甲苯中,苯环上的一硝基代物有1种,共9种,可能结构有2种,故D错误.
故选A.
点评 本题主要考查有机物的同分异构体的书写,注意结构的判断和书写方法是关键,难度中等.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | NaHCO3溶液中加入盐酸:CO32-+2H+═H2O+CO2↑ | |
| C. | 向硫酸溶液中加入Ba(OH)2溶液:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | 偏铝酸钠溶液中通入过量二氧化碳:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某课外兴趣小组欲利用如图所示装置自制氢氧燃料电池.
某课外兴趣小组欲利用如图所示装置自制氢氧燃料电池.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 10ml | B. | 30ml | C. | 50ml | D. | 70ml |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 压强 SO2转化率 温度 | 1个大气压 | 5个大气压 | 10个大气压 | 15个大气压 |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
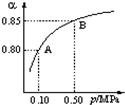 (4)在一个固定容器为5L的密闭容器中充入0.20mol SO2(g)和0.10mol O2(g),t1时刻达到平衡,测得容器中含SO30.18mol.①t1时刻达到平衡后,改变一个条件使化学反应速度发生如图所示的变化,则改变的条件是C.
(4)在一个固定容器为5L的密闭容器中充入0.20mol SO2(g)和0.10mol O2(g),t1时刻达到平衡,测得容器中含SO30.18mol.①t1时刻达到平衡后,改变一个条件使化学反应速度发生如图所示的变化,则改变的条件是C.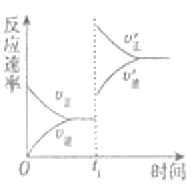
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 按如图进行电解实验(A、B、C、D均为惰性电极).
按如图进行电解实验(A、B、C、D均为惰性电极).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验①和②均能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O72->Fe3+ | |
| C. | CrO42- 和Fe2+在酸性溶液中可以大量共存 | |
| D. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com