
【题目】下列有关说法正确的是
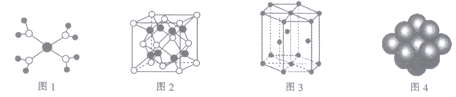
A. 水合铜离子的模型如图1所示,1个水合铜离子中含有4个配位键
B. K2O晶体的晶胞如图2所示,每个K2O晶胞平均占有8个O2-
C. 金属Zn中Zn原子堆积模型如图3所示,空间利用率为68%
D. 金属Cu中Cu原子堆积模型如图4所示,为面心立方最密堆积,每个Cu原子的配位数均为8
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s) = CuSO4(s)+5H2O(l) △H=+Q2 kJ·mol1则Q1、Q2的关系为
A.Q1<Q2 B.Q1>Q2 C.Q1=Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,美国正在研究用锌电池取代目前广泛使用的蓄电池,它具有容量大、污染小的特点,其电池反应为:2Zn+O2=2ZnO ,其原料为锌、空气和电解质溶液,则下列叙述正确的是
A.锌为正极,空气在负极反应
B.负极还原反应,正极氧化反应
C.负极的电极反应为:Zn-2e-+2OH-=ZnO+H2O
D.电池工作时溶液的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对元素周期表说法不正确的是( )
A. 在第ⅥB和第ⅦB族附近可以找到耐高温金属材料
B. 第ⅣA族所有含氧酸的钠盐,溶于水均呈碱性
C. 如果已知元素的最外层电子数为2,由此不能判断该元素在周期表中的位置
D. 目前已知发现的第ⅣA族元素为5种,所以该族元素共有5种单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用比表示阿伏加德罗常数的数值,下列说法正确的是( )
A.ILlmol/L的氯化铁溶液中,若C1-的数目为3 NA,则Fe3+的数目为NA
B.1 molN2和3 molH2在一定条件下充分反应,转移电子数目为6NA
C.常温下,1L0.lmol/L的Na2S溶液中阴离子数目大于0.1 NA
D.0.1 mol Cl2通入水中,转移电子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二锰(Mn2O3)在现代工业上应用广泛,在锂离子电池的制备中有重要的作用。用软锰矿(主要成分为MnO2)和硫锰矿(主要成分为MnS)制备高纯度Mn2O3的工艺流程如图所示。
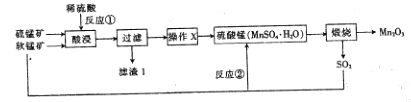
(1)反应①中会生成一种非金属单质,则该非金属单质是_________________,该反应的还原剂是________________。(填化学式)
(2)操作X为蒸发浓缩、__________、过滤、洗涤烘干。在洗涤操作中,常用酒精洗涤MnSO4·H2O晶体,主要目的是________________;
(3)Mn2O3与MnO2类似,加热时也能与浓盐酸反应放出Cl2,该反应的离子方程式为_____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是地壳中含量最高的金属元素,其单质及化合物在生产生活中有广泛的应用。
(1)普通水泥的主要成分之一是铝酸三钙(3CaO·Al2O3),3CaO·Al2O3中Al的化合价为__________;
(2)氯化铝广泛用于有机合成和石油工业的催化剂。将铝土矿粉(Al2O3)与炭粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式__________;
(3)现将一定量的铝粉和镁粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐渐加入4mol·L-1的NaOH溶液,加入NaOH溶液的体积(mL)与产生沉淀的质量的关系如图所示。
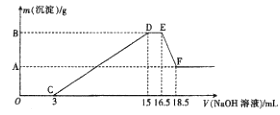
①D→E过程中反应的离子方程式为____________________;
②A点对应纵坐标的数值是__________,原稀硝酸的浓度是__________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用NaOH固体和蒸馏水准确配制一定物质的量浓度的NaOH溶液,以下仪器中不需要用到的是( )
A. 烧瓶 B. 烧杯 C. 容量瓶 D. 玻璃棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用离子方程式Ba2++SO42- ===BaSO4↓表示的是
A. 氯化钡和硫酸钠溶液反应 B. 碳酸钡和稀硫酸反应
C. 氢氧化钡和硫酸铝溶液反应 D. 氢氧化钡和稀硫酸反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com