
【题目】有A、B、C、D、E、F六种物质,它们的相互转化关系如下图(反应条件略,有些反应的产物和反应的条件没有全部标出)。已知A、B、E是单质,其中A着火只能用干燥的沙土灭火,B在常温下为气体,C俗名称为烧碱,D为无色无味液体。

(1)写出A、B、F的化学式 A______ B ______ F ______。
(2)写出A和D反应生成B和C的化学方程式_____________。若生成3mol的B,则转移的电子数目为_______________ 。
(3)写出E与C、D反应生成的B和F离子方程式____________________________。
【答案】Na H2 NaAlO2 2Na+2H2O=2NaOH+H2 ![]() 6NA 2Al+2H2O+2OH-=2AlO2-++3H2
6NA 2Al+2H2O+2OH-=2AlO2-++3H2 ![]()
【解析】
有A、B、C、D、E、F六种物质,C俗名称为烧碱,C为NaOH;D为无色无味液体,D为H2O,根据框图,单质A与水反应生成一种气体单质B和NaOH,则A为Na,B为H2,氢氧化钠和水与单质E反应生成氢气,则E为Al,因此F为偏铝酸钠,据此答题。
(1)根据上述分析,A、B、F的化学式分别为:Na、H2、NaAlO2,故答案为:Na、H2、NaAlO2。
(2)钠和水反应的化学方程式为:2Na+2H2O=2NaOH+H2![]() ,该反应中每生成1mol的氢气,转移2mol电子,若生成3mol的H2,则转移的电子数目为6NA,故答案为:2Na+2H2O=2NaOH+H2
,该反应中每生成1mol的氢气,转移2mol电子,若生成3mol的H2,则转移的电子数目为6NA,故答案为:2Na+2H2O=2NaOH+H2![]() ,6NA。
,6NA。
(3)铝与氢氧化钠溶液反应的离子方程式为:2Al+2H2O+2OH-=2AlO2-++3H2![]() ,故答案为:2Al+2H2O+2OH-=2AlO2-++3H2
,故答案为:2Al+2H2O+2OH-=2AlO2-++3H2![]() 。
。


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】能在水溶液中大量共存的离子组是( )
A. H+、Fe3+、SO42-、I- B. H+、NH4+、HCO3-、NO3-
C. Ag+、K+、Cl-、SO42- D. K+、AlO2-、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电解法处理含镍酸性废水并得到单质镍的原理如图所示,已知:①Ni2+在弱酸性溶液中发生水解②氧化性:Ni2+(高浓度)>H+ >Ni2+(低浓度)。下列说法正确的是

A. 碳棒上发生的电极反应:2C1--2e-=Cl2 ↑
B. 电解过程中,B中NaCl 溶液的浓度将不断减小
C. 为了提高Ni的产率,电解过程中需要控制废水的pH
D. 若将图中阳离子交换膜去掉,则电解反应总方程式不发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用图1 和图2中的信息,按图3装置(连接的A、B瓶中已充有NO2气体)进行实验。下列说法正确的是
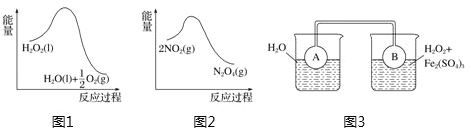
A. H2O2中只含有极性共价键,不含离子键
B. 2NO2![]() N2O4的平衡常数K随温度升高而减小
N2O4的平衡常数K随温度升高而减小
C. 向H2O2中加入Fe2(SO4)3后,B中颜色变浅
D. H2O2分解反应中Fe2(SO4)3作催化剂,可以使反应的△H减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合动力汽车(HEV)中使用了镍氢电池,其工作原理如图所示其中M为储氢合金,MH为吸附了氢原子的储氢合金,KOH溶液作电解液。关于镍氢电池,下列说法不正确的是

A. 充电时,阴极附近pH降低
B. 电动机工作时溶液中OH-向甲移动
C. 放电时正极反应式为: NiOOH+H2O+e- = Ni(OH)2+OH-
D. 电极总反应式为:M+Ni(OH)2 = MH+NiOOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(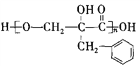 )为一种高分子树脂,其合成路线如下:
)为一种高分子树脂,其合成路线如下:
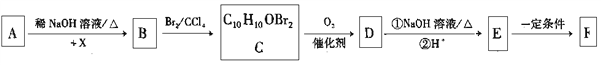
已知:①A为苯甲醛的同系物,分子中无甲基,其相对分子质量为134;
②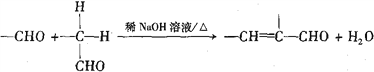
请回答下列问题:
(1)X的化学名称是_________________。
(2)E生成F的反应类型为_________________。
(3)D的结构简式为_________________。
(4)由B生成C的化学方程式为_________________。
(5)芳香族化合物Y是D的同系物,Y的同分异构体能与饱和Na2CO3溶液反应放出气体,分子中只有1个侧链,核磁共振氢普显示有5种不同化学环境的氢,峰值面积比为6:2:2:1:1。写出两种符合要求的Y的结构简式___________、__________。
(6)写出以甲醛、丙醛和乙二醇为主要原料合成软质隐形眼镜高分子材料—聚甲基丙烯酸羟乙酯(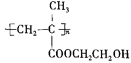 )的合成路线(无机试剂自选):_________________。
)的合成路线(无机试剂自选):_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用 过量稀硝酸处理后沉淀量减少到4.66g,并有气体放出。试计算:
(1)原混合溶液中Na2CO3和Na2SO4的物质的量浓度_______________;
(2)产生的气体在标准状况下的体积_____________。(要有过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 作为一种重要的化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究着被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
作为一种重要的化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究着被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
反应Ⅰ:![]()
![]()
![]() △H=
△H=![]()
反应Ⅱ:![]()
![]()
![]()
![]()
(1)在恒温恒容装置中充入一定量的![]() 和
和![]() ,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是___________________。
,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是___________________。
A. 使用催化剂时,可降低该反应的活化能,加快其反应速率
B. 若测得容器内![]() 时,说明反应已达平衡
时,说明反应已达平衡
C. 当容器内![]() 时,说明反应已达平衡
时,说明反应已达平衡
D. 当测得容器内氧气浓度不再变化时,说明反应已达达平衡
(2)氨催化氧化时会发生上述两个竞争反应Ⅰ、Ⅱ。为分析某催化剂对该反应的选择性,1L密闭容器中充入1 mol ![]() 和2 mol
和2 mol ![]() ,测得有关物质的量关系如图
,测得有关物质的量关系如图
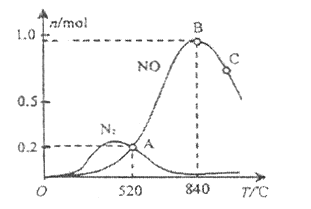
①该催化剂在高温时选择反应_______________(填“Ⅰ”或“Ⅱ”)。
②520℃时, ![]()
![]()
![]() 的平衡常数K表达式________。
的平衡常数K表达式________。
③有利于提高![]() 转化为
转化为![]() 的速率的措施有_________________。
的速率的措施有_________________。
A. 使用催化剂![]()
B. 将反应生成的![]() 及时移出
及时移出
C. 充入稀有气体
D. 投料比不变,增加反应物的浓度
E. 降低反应温度
(3)最近华南理工大提出利用电解法制![]() 并用产生的
并用产生的![]() 处理废氨水,装置如图
处理废氨水,装置如图
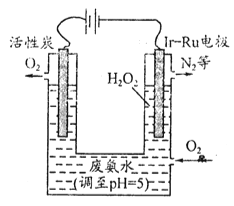
①为了不影响![]() 的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)_________c(NO3-)(填>、=、<)。
的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)_________c(NO3-)(填>、=、<)。
②Ir-Ru惰性电极有吸附![]() 作用,该电极上产生
作用,该电极上产生![]() 的反应为_________,生成的
的反应为_________,生成的![]() 与废液反应的离子方程式为_________________。
与废液反应的离子方程式为_________________。
③理论上电路中每转移3 mol电子,最多可以处理![]() 的物质的量为__________。
的物质的量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4,硼为+3价)为白色粉末,在干燥空气中稳定,在潮湿空气中分解,是常用的还原剂。偏硼酸钠(NaBO2)易溶于水,不溶于乙醇,易水解。目前有多种工艺制备NaBH4 。
(1)用硼精矿(含有一定量B2O3,及Al2O3、SiO2、Fe2O3等杂质)制取NaBH4的流程如下:

①“溶解”时,B2O3与NaOH反应生成了NaBO2,反应离子方程式为_____________。
②“除硅铝”步骤加入CaO,而不加入CaCl2的原因有:能将硅、铝以沉淀除去;尽量不带入杂质离子;__________。
③“操作2”是将滤液蒸发、结晶、洗涤,其中洗涤选用的试剂最好是___________。
④“反应1”是MgH2与NaBO2混合得到NaBH4和MgO,其化学方程式为_________。
(2)我国孙彦平采用耐腐蚀电极材料,以阳离子交换膜为隔离膜,电解偏硼酸钠的碱溶液,也可以高效制备NaBH4。该工艺阳极产物为______,阴极电极方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com