
| A. | 碳酸钙溶于醋酸 CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯化铁溶液溶解铜 Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 氯气溶于水 Cl2+H2O═2H++Cl-+ClO- | |
| D. | 氢氧化钠溶液吸收二氧化硫气体 SO2+2OH-═SO42-+H2O |
分析 A.醋酸为弱酸,保留化学式;
B..二者反应生成氯化亚铁和氯化铜;
C.次氯酸为弱酸,应保留化学式;
D.原子个数不守恒;
解答 解:A.碳酸钙溶于醋酸,离子方程式:CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO-,故A错误;
B.氯化铁溶液溶解铜,离子方程式:Cu+2Fe3+═Cu2++2Fe2+,故B正确;
C.氯气溶于水,离子方程式:Cl2+H2O═H++Cl-+HClO,故C错误;
D.氢氧化钠溶液吸收二氧化硫气体,反应生成亚硫酸钠和水,离子方程式:SO2+2OH-═SO32-+H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应遵循客观事实、遵循原子个数、电荷数守恒规律,注意化学式的拆分.


科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:选择题
氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮的化合价为+3
D.AlN的摩尔质量为41 g
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “Cu-Zn-硫酸”原电池中,电子从Zn经过导线到达Cu,再经过溶液回到Zn形成闭合回路 | |
| B. | “Al-Mg-NaOH”原电池中,活泼型强的Mg失去电子,被氧化,做负极 | |
| C. | 理论上所有自发进行的氧化还原反应均可设计成原电池 | |
| D. | 已知铅蓄电池总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,可推负极是反应是 Pb-2e-=Pb2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
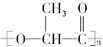 ,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )
,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )| A. | 降解塑料是一种纯净物 | |
| B. | 其生产过程中的聚合方式与聚苯乙烯相似 | |
| C. | 它属于一种线型高分子材料 | |
| D. | 其相对分子质量为72 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
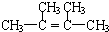 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16 g O2所含的原子数目为NA | |
| B. | 0.5 mol H2O2含有的原子数目为1.5NA | |
| C. | 1 mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com