
【题目】X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+3、+5、+7,核电荷数按照Z、X、Y、W的顺序增大。已知Z的原子次外层的电子数为2,W、X原子次外层电子数为8。
(1)请写出元素Y的原子结构示意图_______________;其中元素W在周期表中的位置_______________________________。
(2)用电子式表示X在空气中生成的氧化物的形成过程:__________________________。
(3)X、Y、Z、W的原子半径由大到小的顺序为:_____________________________。(用元素符号表示)
(4)请写出W的单质与X的最高价氧化物对应水化物反应的离子方程式:_______________________________。
(5)写出Z与氢元素形成的10电子微粒化学式_____________________(任写两种)。
(6)元素X与元素Y相比,金属性较强的是_____(用元素符号表示),请举一例实验事实证明这一结论__________________________________________________________。
【答案】 第三周期第ⅦA族
第三周期第ⅦA族 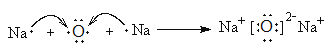 Na>Al>Cl>N Cl2+ 2OH-= Cl-+ ClO-+H2O NH3、NH4+、NH2- Na Na与水反应要比Al剧烈(其它合理答案也可)
Na>Al>Cl>N Cl2+ 2OH-= Cl-+ ClO-+H2O NH3、NH4+、NH2- Na Na与水反应要比Al剧烈(其它合理答案也可)
【解析】
Z的原子次外层的电子数为2,最高价是+5价,所以Z是氮元素。核电荷数按照Z、X、Y、W的顺序增大,且W、X原子次外层电子数为8,所以根据其最高价可知,W是氯元素,X是Na,则Y是Al。据此分析解答。
(1)Al的原子序数是13,所以原子结构示意图为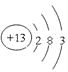 。氯元素的原子序数是17,所以位于第三周期第ⅦA族。
。氯元素的原子序数是17,所以位于第三周期第ⅦA族。
(2)钠在空气中生成氧化钠,含有离子键的离子化合物,所以其形成过程是
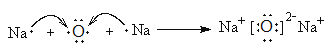 。
。
(3)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,所以X、Y、Z、W的原子半径由大到小的顺序为Na>Al>Cl>N。
(4)氯气和氢氧化钠溶液反应的离子方程式是Cl2+ 2OH-= Cl-+ ClO-+H2O。
(5)氮元素和氢元素形成的10电子微粒有NH3、NH4+、NH2-等。
(6)由于钠极易和水生成氢气和氢氧化钠,而A和水是不反应的,所以钠的金属性强于铝的金属性。


科目:高中化学 来源: 题型:
【题目】磷酸二氢钾(KH2PO4)在工业、农业、医药及食品等行业均有广泛的应用。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如图所示(部分流程步骤已省略):

其中,萃取是因为KCl和H3PO4产生的HCl易溶于有机萃取剂。请回答下列问题:
(1)氟磷灰石(Ca5P3FO12)中磷元素的化合价是____。
(2)用化学反应原理解释KCl和H3PO4生成KH2PO4的原因: ________。
(3)沸腾槽不能采用陶瓷材质的原因是_______(用化学方程式表示)。
(4)在得到N的流程中“……”的操作步骤是______、洗涤、干燥。
(5)在萃取过程中,影响萃取率的因素复杂,下图是投料比![]() 对萃取率的影响曲线,在实际操作中,应选择投料比
对萃取率的影响曲线,在实际操作中,应选择投料比![]() 的范围是___(填序号)。
的范围是___(填序号)。

A.0.2~0.4 B.0.4~0.6 C.0.6~0.8 D.0.8~1.0 E.1.0~1.2
(6)电解法制备KH2PO4是用石墨作电极,将电解槽分为a区和b区,中间用阳离子交换膜隔离,a区为3 mol·L-1 H3PO4,b区为3 mol·L-1 KCl。阳极区为____(填“a”或“b”)区,其电极反应式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据如图所示实验装置,回答下列问题:

![]() 写出下列仪器的名称:
写出下列仪器的名称:![]() ______;
______;
![]() 若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器有______,将仪器补充完整后进行的实验操作的名称为______;
若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器有______,将仪器补充完整后进行的实验操作的名称为______;![]() 的进水口是______
的进水口是______![]() 填f或
填f或![]()
![]() 某同学用装置Ⅱ配制
某同学用装置Ⅱ配制![]() NaCl溶液,指出图中的错误操作______.
NaCl溶液,指出图中的错误操作______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前工业合成氨的原理是N2(g)+3H2(g)![]() 2NH3(g) △H=-93.0kJ·mol-1
2NH3(g) △H=-93.0kJ·mol-1
(1)已知一定条件下:2N2(g)+6H2O(l)![]() 4NH3(g)+3O2(g) △H=+l 530.0kJ·mol一1。则氢气燃烧热的热化学方程式为___。
4NH3(g)+3O2(g) △H=+l 530.0kJ·mol一1。则氢气燃烧热的热化学方程式为___。
(2)如图,在恒温恒容装置中进行合成氨反应。

①表示N2浓度变化的曲线是____。
②前25min内,用H2浓度变化表示的化学反应速率是____。
③在25min末刚好平衡,则平衡常数K=____。
(3)在恒温恒压装置中进行工业合成氨反应,下列说法正确的是___。
A.气体体积不再变化,则已平衡
B.气体密度不再变化,尚未平衡
C.平衡后,往装置中通入一定量Ar,压强不变,平衡不移动
D.平衡后,压缩容器,生成更多NH3
(4)电厂烟气脱氮的主反应①:4NH3(g)+6NO(l)![]() 5N2(g)+6H2O(g) △H<0,副反应②:2NH3(g)+8NO(g)
5N2(g)+6H2O(g) △H<0,副反应②:2NH3(g)+8NO(g)![]() 5N2O(g)+3H2O(g)△H>0。平衡混合气中N2与N2O含量与温度的关系如图。
5N2O(g)+3H2O(g)△H>0。平衡混合气中N2与N2O含量与温度的关系如图。

请回答:在400~600K时,平衡混合气中N2含量随温度的变化规律是___,导致这种规律的原因是___(任答合理的一条原因)。
(5)直接供氨式燃料电池是以NaOH溶液为电解质溶液,电池反应为4NH3(g)+3O2=2N2+6H2O。则负极电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积,不同浓度的NaCl、MgCl2、AlCl3三种溶液分别与等体积等物质和量浓度的AgNO3溶液恰好完全反应,则NaCl、MgCl2、AlCl3三种溶液中Cl-的物质的量浓度之比是
A.1:2:3B.3:2:1C.6:3:2D.1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:
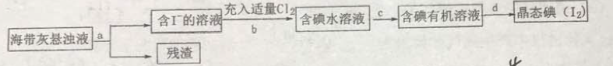
(1)指出提取碘的过程中有关的实验操作名称:a__________,c__________。
(2)操作c需要的仪器是__________,所用的有机试剂可以是CCl4,简述选择理由__________;最后碘的CCl4溶液是通过__________获得(填“漏斗上口”或“漏斗下口”)。
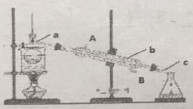
(3)从含碘的有机溶液中提取碘和回收有机溶液CCl4,还需要经过__________,观察下图所示实验装置,指出仪器名称b__________,冷却水从__________进入(填A或B),最后碘留在__________里。(填仪器名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2NO2(g)![]() N2 O4(g);△H= -57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
N2 O4(g);△H= -57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
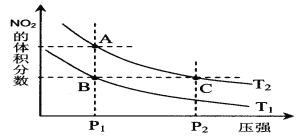
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A浅,C深
C.由状态A到状态B,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①AgCl②铜③液态醋酸④CO2⑤H2SO4⑥Ba(OH)2固体⑦NaHCO3⑧稀硝酸⑨熔融FeCl3 ⑩NaHSO4
(1)上述状态下可导电的是_________;(填序号,下同)属于强电解质的是________;属于非电解质的是______.
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH﹣═H2O,该离子反应对应的化学方程式为_______________________________
(3)用⑨的饱和溶液制备Fe(OH)3胶体的离子方程式_______________________ 足量的④通入⑥的溶液中的离子方程式______________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟“侯氏制碱法”原理,以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为NH3+CO2+H2O=NH4HCO3;NH4HCO3+NaCl=NaHCO3↓+NH4Cl;2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。
(1)利用上述反应原理,设计如图所示装置,制取碳酸氢钠晶体,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去。

①E中制备气体时,所需药品是___(填字母)。
a.石灰石 b.生石灰 c.稀盐酸 d.浓氨水
②B中应盛有___溶液。在实验过程中,应向C中先通入足量的__。
③E装置向C中通气的导管不能插入液面下的原因是___。
(2)该小组同学为了测定C中所得碳酸氢钠晶体的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为4g。再将晶体加热到质量不再变化时,称量所得粉末质量为mg。然后进行如图所示实验:
![]()
![]()
![]()
![]()
![]()
![]()
①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,正确的实验操作是:在加入氯化钙溶液后,___。
②操作Ⅲ涉及的步骤名称为___、___、干燥。
③所得晶体中碳酸氢钠的纯度为____%。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com