
”¾ĢāÄæ”æŌĖÓĆĖłŃ§»ÆѧŌĄķ£¬½ā¾öĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŅŃÖŖ£ŗSi+2NaOH+H2OØTNa2SiO3+2H2 £® ijĶ¬Ń§ĄūÓƵ„ÖŹ¹čŗĶĢśĪŖµē¼«²ÄĮĻÉč¼ĘŌµē³Ų£ØNaOHĪŖµē½āÖŹČÜŅŗ£©£¬øĆŌµē³Ųøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£»
£Ø2£©ŅŃÖŖ£ŗ¢ŁC£Øs£©+O2£Øg£©ØTCO2£Øg£©”÷H=a kJmol©1£»¢ŚCO2£Øg£©+C£Øs£©ØT2CO£Øg£©”÷H=b kJmol©1£»¢ŪSi£Øs£©+O2£Øg£©ØTSiO2£Øs£©”÷H=c kJmol©1 £® ¹¤ŅµÉĻÉś²ś“Ö¹čµÄČČ»Æѧ·½³ĢŹ½ĪŖ£»
£Ø3£©ŅŃÖŖ£ŗCO£Øg£©+H2O£Øg£©H2£Øg£©+CO2£Øg£©£®±ķĪŖøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČŹ±µÄĘ½ŗā³£Źż£®Ōņ£ŗøĆ·“Ó¦µÄ”÷H0£ØĢī”°£¼”±»ņ”°£¾”±£©£»500”ꏱ½ųŠŠøĆ·“Ó¦£¬ĒŅCOŗĶH2OĘšŹ¼ÅضČĻąµČ£¬COĘ½ŗā×Ŗ»ÆĀŹĪŖ £®
ĪĀ¶Č”ę | 400 | 500 | 800 |
Ę½ŗā³£ŹżK | 9.94 | 9 | 1 |
”¾“š°ø”æ
£Ø1£©Si+6OH©©4e©=SiO32©+3H2O
£Ø2£©2C£Øs£©+SiO2£Øs£©=Si£Øs£©+2CO£Øg£©”÷H=£Øa+b©c£©kJ?mol©1
£Ø3£©£¼£»75%
”¾½āĪö”æ½ā£ŗ£Ø1£©øŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬SiŌŚøŗ¼«ÉĻŹ§Č„µē×Ó£¬¼īŠŌĢõ¼žĻĀÉś³É¹čĖįøłÓėĖ®£¬øŗ¼«µē¼«·“Ó¦Ź½ĪŖ£ŗSi+6OH©©4e©=SiO32©+3H2O£¬
ĖłŅŌ“š°øŹĒ£ŗSi+6OH©©4e©=SiO32©+3H2O£»
£Ø2.£©ŅŃÖŖ£ŗ¢ŁC£Øs£©+O2£Øg£©ØTCO2£Øg£©”÷H=a kJmol©1£»
¢ŚCO2£Øg£©+C£Øs£©ØT2CO£Øg£©”÷H=b kJmol©1£»
¢ŪSi£Øs£©+O2£Øg£©ØTSiO2£Øs£©”÷H=c kJmol©1 £¬
øł¾ŻøĒĖ¹¶ØĀÉ£¬¢Ł+¢Ś©¢ŪµĆ£ŗ2C£Øs£©+SiO2£Øs£©=2CO£Øg£©+Si£Øs£©”÷H=£Øa+b©c£© kJmol©1 £¬
ĖłŅŌ“š°øŹĒ£ŗ2C£Øs£©+SiO2£Øs£©=2CO£Øg£©+Si£Øs£©”÷H=£Øa+b©c£© kJmol©1£»
£Ø3.£©ÓɱķÖŠŹż¾ŻæÉÖŖ£¬ÉżøßĪĀ¶Č£¬Ę½ŗā³£Źż¼õŠ”£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬¼“”÷H£¼0£»
COŗĶH2OĘšŹ¼ÅضČĻąµČ£¬ĮīĖūĆĒµÄĘšŹ¼ÅضČĪŖ1mol/L£¬ÉčĘ½ŗāŹ±COµÄÅØ¶Č±ä»ÆĮæĪŖxmol/L£¬Ōņ£ŗ
CO£Øg£© | + | H2O£Øg£© | ØT | H2£Øg£© | + | CO2£Øg£© | |
æŖŹ¼£Ømol/L£©£ŗ | 1 | 1 | 0 | 0 | |||
×Ŗ»Æ£Ømol/L£©£ŗ | x | x | x | x | |||
Ę½ŗā£Ømol/L£©£ŗ | 1-x | 1©x | x | x |
¹Ź ![]() =9£¬½āµĆx=0.75£¬
=9£¬½āµĆx=0.75£¬
¹ŹCOµÄ×Ŗ»ÆĀŹ= ![]() ”Į100%=75%£¬
”Į100%=75%£¬
ĖłŅŌ“š°øŹĒ£ŗ£¼£»75%£®
”¾æ¼µć¾«Īö”æ½ā“š“ĖĢāµÄ¹Ų¼üŌŚÓŚĄķ½ā»ÆŃ§Ę½ŗāµÄ¼ĘĖćµÄĻą¹ŲÖŖŹ¶£¬ÕĘĪÕ·“Ó¦Īļ×Ŗ»ÆĀŹ=×Ŗ»ÆÅØ¶Č”ĀĘšŹ¼ÅØ¶Č”Į100%=×Ŗ»ÆĪļÖŹµÄĮæ”ĀĘšŹ¼ĪļÖŹµÄĮæ”Į100%£»²śĘ·µÄ²śĀŹ=Źµ¼ŹÉś³É²śĪļµÄĪļÖŹµÄĮæ”ĀĄķĀŪÉĻæɵƵ½²śĪļµÄĪļÖŹµÄĮæ”Į100%£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņĢśæóÓÖ³Ę»ĘĢśæó£¬ŹĒÉś²śĮņĖįµÄŌĮĻ£¬ĘäÖ÷ŅŖ³É·ÖĪŖFeS2.850”ꔫ900”ꏱ£¬ĮņĢśæóŌŚŃõĘųÖŠģŃÉÕ£¬æÉÄÜ·¢ÉśĻĀĮŠ·“Ó¦£Ø¼ŁÉčæÕĘųÖŠµÄN2ŗĶO2Ģå»ż±ČĪŖ4£ŗ1£©¢Ł3FeS2+8O2”śFe3O4+6SO2 ¢Ś4FeS2+11O2”ś2Fe2O3+8SO2
£Ø1£©ŗ¬Įņ35%µÄĮņĢśæóѳʷ£ØŌÓÖŹ²»ŗ¬Įņ£©£¬ĘäFeS2µÄŗ¬ĮæĪŖ £®
£Ø2£©Ä³ĮņĖį³§ĆæĢģÓĆŗ¬FeS260%µÄĮņĢśæó500tÉś²śĮņĖį£¬Čē¹ūŌŚ·ŠĢŚĀÆÄŚĖšŹ§5%µÄĮņ£¬SO2µÄ×Ŗ»ÆĀŹĪŖ90%£®ĆæĢģÄÜÉś²ś98%µÄĮņĖį¶Ö
£Ø3£©ĮņĢśæóģŃÉÕ¹ż³ĢÖŠæÕĘųÓĆĮæ²»Ķ¬Ź±£¬·¢Éś·“Ó¦ŗĶÉś³ÉĀÆĘųÖŠSO2ŗ¬ĮæŅ²²»Ķ¬£¬ŗ¬FeS2 72%µÄĮņĢśæóŌŚæÕĘųÖŠģŃÉÕ²¢°“·“Ó¦¢ŁĶźČ«·“Ó¦£¬ĮŠŹ½¼ĘĖćĀÆĘųÖŠµÄSO2µÄĢå»ż·ÖŹż×ī“óĪŖ¶ąÉŁ£æ
£Ø4£©ĪŖČ·±£SO2×Ŗ»ÆĪŖSO3µÄ×Ŗ»ÆĀŹ£¬Ä³ĮņĖį³§Ź¹ÓĆø»ŃõæÕĘų£ØæÕĘųÖŠ¼Ó“æŃõ£©ģŃÉÕĮņĢśæó£¬ĀÆĘųÖŠSO2ŗĶO2µÄĢå»ż·ÖŹż·Ö±š“ļµ½11%ŗĶ9%£¬FeS2ĶźČ«×Ŗ»ÆĪŖFe2O3 £¬ ĮŠŹ½¼ĘĖćø»ŃõæÕĘųÖŠµÄŃõĘųĢå»ż·ÖŹżĪŖ¶ąÉŁ£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŚČżÖÜĘŚŌŖĖŲX,Y,Z,WµÄ×īøß¼ŪŃõ»ÆĪļČÜÓŚĖ®æɵĆĖÄÖÖČÜŅŗ£¬0.010molL©1µÄÕāĖÄÖÖČÜŅŗpHÓėøĆŌŖĖŲŌ×Ó°ė¾¶µÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £© 
A.ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗZ£¾W£¾Y
B.¼ņµ„Ąė×Ó°ė¾¶£ŗZ£¼W
C.YŌŖĖŲ“ęŌŚĶ¬ĖŲŅģŠĪĢå
D.XŗĶYµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĒ”ŗĆÖŠŗĶŹ±£¬ČÜŅŗ³ŹÖŠŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĢžÓėĒāĘų·¢Éś·“Ó¦ŗóÄÜÉś³É£ØCH3£©2CHCH2CH3 £¬ ŌņøĆĢž²»æÉÄÜŹĒ£Ø £©
A.2©¼×»ł©2©¶”Ļ©
B.2£¬3©¶ž¼×»ł©1©¶”Ļ©
C.3©¼×»ł©1©¶”Ļ©
D.2©¼×»ł©1£¬3©¶”¶žĻ©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌŅŅČ²ĪŖŌĮĻæÉŅŌŗĻ³É¾ŪĀČŅŅĻ©”¢¾Ū±ūĻ©ėęŗĶĀȶ”Ļš½ŗ£¬ÓŠ¹ŲŗĻ³ÉĀ·ĻßĶ¼ČēĻĀ£ŗ 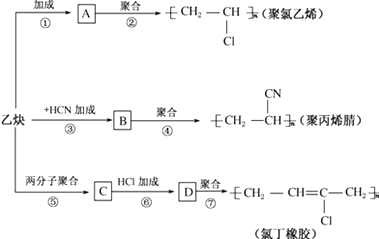
ĒėĶź³ÉĻĀĮŠø÷Ģā£ŗ
£Ø1£©Š“³öĪļÖŹµÄ½į¹¹¼ņŹ½£ŗA £¬ C£»
£Ø2£©Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
·“Ó¦¢Ł£ŗ£»
·“Ó¦¢Ū£ŗ£»
·“Ó¦¢ß£ŗ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĮāĆĢæó£ØÖ÷ŅŖŗ¬MnCO3”¢FeCO3”¢Al2O3”¢SiO2£©ÖʱøMnSO4H2OµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
¢ń£®ĻņĮāĆĢæóÖŠ¼ÓČė¹żĮæĻ”H2SO4 £¬ ¹żĀĖ£»
¢ņ£®ĻņĀĖŅŗÖŠ¼ÓČė¹żĮæMnO2 £¬ ¹żĀĖ£»
¢ó£®µ÷½ŚĀĖŅŗpH=a£¬¹żĀĖ£»
¢ō£®ÅØĖõ”¢½į¾§”¢·ÖĄė”¢øÉŌļµĆµ½²śĘ·£»
¢õ£®¼ģŃé²śĘ·“æ¶Č£®
£Ø1£©²½Öč¢ńÖŠ£¬ĀĖŌüµÄÖ÷ŅŖ³É·ÖŹĒ
£Ø2£©½«MnO2Ńõ»ÆFe2+µÄĄė×Ó·½³ĢŹ½²¹³äĶźÕū£ŗ MnO2+ Fe 2++ ØT Mn 2++ Fe 3++
£Ø3£©ÓėŃ”ÓĆCl2×÷ĪŖŃõ»Æ¼ĮĻą±Č£¬MnO2µÄÓÅŹĘÖ÷ŅŖŌŚÓŚ£ŗŌĮĻĄ“Ō“¹ć”¢³É±¾µĶ”¢æɱÜĆā»·¾³ĪŪČ¾”¢ £®
£Ø4£©ŅŃÖŖ£ŗÉś³ÉĒāŃõ»ÆĪļ³ĮµķµÄpH
Al£ØOH£©3 | Fe£ØOH£©2 | Fe£ØOH£©3 | Mn£ØOH£©2 | |
æŖŹ¼³ĮµķŹ± | 3.4 | 6.3 | 1.5 | 7.6 |
ĶźČ«³ĮµķŹ± | 4.7 | 8.3 | 2.8 | 10.2 |
×¢£ŗ½šŹōĄė×ÓµÄĘšŹ¼ÅضČĪŖ0.1mol/L
²½Öč¢óÖŠaµÄȔֵ·¶Ī§ŹĒ £®
£Ø5£©²½Öč¢õ£¬Ķعż²ā¶Ø²śĘ·ÖŠĆĢŌŖĖŲµÄÖŹĮæ·ÖŹżĄ“ÅŠ¶Ļ²śĘ·“æ¶Č£®
ŅŃÖŖŅ»¶ØĢõ¼žĻĀ£¬MnO4©ÓėMn2+·“Ӧɜ³ÉMnO2 £® Č”x g²śĘ·Åä³ÉČÜŅŗ£¬ÓĆ0.1mol/L KMnO4ČÜŅŗµĪ¶Ø£¬ĻūŗÄKMnO4ČÜŅŗy mL£¬²śĘ·ÖŠĆĢŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2005ğƥ¹ś»Æѧ»įæƱصĄ£¬ĆĄ¹ś¶ķĄÕøŌ“óѧµÄ»Æѧ¼ŅŹ¹ÓĆĮĖŅ»ÖÖŠĀŠĶ“߻ƼĮ£¬ŌŚ³£ĪĀ³£Ń¹ĻĀŗĻ³É°±£¬·“Ó¦æɱķŹ¾ĪŖN2+3H2 ![]() 2NH3”÷H£¼0£¬ÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø £©
2NH3”÷H£¼0£¬ÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.øĆ·“Ó¦”÷H£¼0£¬”÷S£¼0£¬ŌŚČĪŗĪĢõ¼žĻĀ¾łæÉ×Ō·¢½ųŠŠ
B.ŠĀ·ØŗĻ³É°±²»ŠčŅŖŌŚøßĪĀĢõ¼žĻĀ£¬æɽŚŌ¼“óĮæÄÜŌ“£¬¼«¾ß·¢Õ¹Ō¶¾°
C.ŠĀ·ØŗĻ³É°±ÄÜŌŚ³£ĪĀĻĀ½ųŠŠŹĒŅņĪŖ²»ŠčŅŖ¶ĻĮŃ»Æѧ¼ü
D.Ź¹ÓĆ“ĖŠĀŠĶ“߻ƼĮÄÜČĆøĆ·“Ó¦½ųŠŠĶźČ«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø5·Ö£©¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŗĖµēŗÉŹżŅĄ“ĪŌö“ó£¬X”¢ZĶ¬Ö÷×壬Z”¢WĶ¬ÖÜĘŚ£¬ĖÄÖÖŌŖĖŲµÄŌ×ÓŠņŹżÖ®ŗĶĪŖ37£¬ŌŚÖÜĘŚ±ķÖŠXŹĒŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£¬YµÄ×īĶā²ćµē×ÓŹżŹĒÄŚ²ćµē×ÓŹżµÄ3±¶”£
£Ø1£©WŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ ”£
£Ø2£©XÓėY ÄÜŠĪ³É¾ßÓŠ18øöµē×ӵĻÆŗĻĪļ£¬“Ė»ÆŗĻĪļµÄµē×ÓŹ½ĪŖ ”£
£Ø3£©X”¢Y”¢ZČżÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļÖŠ“ęŌŚµÄ»Æѧ¼üĄąŠĶĪŖ ”£
£Ø4£©Z”¢WĮ½ÖÖŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļČÜŅŗÖ®¼ä·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒĻņ100mLµÄŃĪĖįÖŠÖš½„¼ÓČėNaOHČÜŅŗŹ±£¬ČÜŅŗµÄpH±ä»ÆĶ¼Ļó£®øł¾ŻĶ¼ĻóĖłµĆ½įĀŪÕżČ·µÄŹĒ£Ø £© 
A.ŌĄ“ŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ0.1molL©1
B.æÉŅŌŃ”ŌńŗģÉ«ŹÆČļ×÷ĪŖÖøŹ¾¼Į
C.ĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæÅضČĪŖ0.1molL©1
D.pHĪŖ7Ź±¼ÓČėµÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæĪŖ0.1mol
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com